2014届高考化学二轮复习江苏专用 高考模拟演练1练习卷
下列设备工作时,将化学能转化为热能的是( )。
| A |
B |
C |
D |
 |
 |
 |
 |
| 硅太阳能电池 |
锂离子电池 |
太阳能集热器 |
燃气灶 |
下列有关化学用语表示正确的是( )。
A.CO2的电子式: |
B.质子数为43、中子数为56的Tc原子: |
C.Cl-的结构示意图: |
D.氨基乙酸的结构简式: |
下列各组离子在指定的溶液中能大量共存的是( )。
| A.pH=14的溶液中:Na+、Al3+、Cl-、NO3- |
| B.滴入KSCN溶液显血红色的溶液中:K+、Fe2+、SO42-、Cl- |
| C.c(H+)/c(OH-)=1012的溶液中:NH4+、K+、HCO3-、NO3- |
| D.c(I-)=0.1 mol·L-1的溶液中:Na+、Fe3+、ClO-、SO42- |
下列有关物质的性质或应用的说法正确的是( )。
| A.铝合金是一种混合物,它比纯铝的熔点高 |
| B.水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| C.一定条件下,秸秆可以制得葡萄糖和酒精 |
| D.从海水中得到氯化镁,电解氯化镁溶液可获得Mg |
下列实验操作能够达到实验目的的是( )。
| A.用激光笔鉴别淀粉溶液和蔗糖溶液 |
| B.实验室采用上图所示装置收集SO2 |
| C.除去NaHCO3溶液中的Na2CO3,可加入Ca(OH)2溶液后过滤 |
| D.配制一定物质的量浓度溶液时,容量瓶用蒸馏水洗涤后再用待装溶液润洗 |
NA表示阿伏加德罗常数的值,下列说法正确的是( )。
| A.5.6 g铁粉在0.1 mol氯气中充分燃烧,转移电子数为0.3NA |
| B.常温常压下,1 mol氦气含有的核外电子数为4NA |
| C.7.8 g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA |
| D.0.5 mol雄黄(As4S4,结构如图)含有NA个S—S键 |

下列离子方程式书写不正确的是( )。
| A.NaOH溶液与SO2反应,当n(NaOH)∶n(SO2)=4∶3时,4OH-+3SO2=SO32-+2HSO3-+H2O |
| B.CuCl2溶液与Na2S溶液2∶1反应:Cu2++S2-=CuS↓ |
| C.Cl2与FeBr2溶液反应,当n(Cl2)∶n(FeBr2)=1∶1时:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| D.1 mol·L-1的NaAlO2溶液和2.5 mol·L-1的盐酸等体积互相均匀混合:2AlO2-+5H+=Al(OH)3↓+Al3++H2O |
AlAg2O电池是一种可用作水下动力的优良电源,其原理如图所示。该电池工作时总反应式为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则下列说法错误的是( )。
| A.工作时正极发生还原反应 |
| B.当电极上生成1.08 g Ag时,电路中转移的电子为0.01 mol |
| C.Al电极的反应式为Al-3e-+4OH-=AlO2-+2H2O |
| D.工作时电解液中的Na+透过隔膜移向Al电极 |
X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是
( )。
| A.Y元素最高价氧化物对应的水化物化学式为H3YO4 |
| B.Y最简单气态氢化物的水溶液显弱碱性 |
| C.原子半径由小到大的顺序为:X<Z<Y<W |
| D.X、Z两种元素的氧化物中所含化学键类型相同 |
下列有关说法正确的是( )。
| A.NH4Cl(s)=NH3(g)+HCl(g)室温下不能自发进行,说明该反应的ΔH<0 |
| B.镀锌铁制品镀层破损后,铁制品比受损前更容易生锈,而镀锡铁则相反 |
C.对于N2(g)+3H2(g) 2NH3(g),当其他条件不变时,压缩气体体积使压强增大,正反应和逆反应速率以及H2的平衡转化率均增大 2NH3(g),当其他条件不变时,压缩气体体积使压强增大,正反应和逆反应速率以及H2的平衡转化率均增大 |
| D.100 ℃时水的离子积常数KW为5.5×10-13,说明水的电离是放热反应 |
从一种珊瑚中分离出的活性含氯化合物punaglandin具有很强的抗癌活性,它的结构简式如图,有关该化合物的说法正确的是( )。
| A.分子含有4个手性碳原子 |
| B.能使酸性高锰酸钾溶液褪色 |
| C.分子有3种含氧官能团 |
| D.分子中所有碳原子可以处于同一平面 |
下列有关实验方法和结论都正确的是( )。
| A.酸碱中和滴定时,锥形瓶需用待测液润洗2次,再加入待测液 |
| B.联合制碱法是将二氧化碳和氨气通入饱和氯化钠溶液中生成碳酸钠 |
| C.检验蔗糖水解产物具有还原性:在蔗糖水解后的溶液中先加入适量稀NaOH溶液中和,再加入新制的银氨溶液并水浴加热 |
| D.在浓度均为0.01 mol·L-1的NaCl和Na2CrO4溶液中滴加0.01 mol·L-1AgNO3溶液,先析出AgCl,则Ksp(AgCl)<Ksp(Ag2CrO4) |
T K时,向2.0 L恒容密闭容器中充入1.0 mol COCl2,反应COCl2(g) Cl2(g)+CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
Cl2(g)+CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
| t/s |
0 |
2 |
4 |
6 |
8 |
| n(Cl2)/mol |
0 |
0.16 |
0.19 |
0.20 |
0.20 |
下列说法正确的是( )。
A.反应在前2 s 的平均速率v(CO)=0.080 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时,c(Cl2)=0.11 mol·L-1,则反应的ΔH<0
C.T K时起始向容器中充入0.9 mol COCl2、0.10 mol Cl2和0.10 mol CO,反应达到平衡前v正>v逆
D.T K时起始向容器中充入1.0 mol Cl2和0.9 mol CO,达到平衡时,Cl2的转化率小于80%
下列有关溶液中微粒浓度关系的叙述正确的是( )。
| A.向0.1 mol·L-1NH4Cl溶液中通入一定量氨气后:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B.溶有等物质的量NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C.向CH3COONa溶液中滴加稀盐酸至中性,所得溶液中:c(Cl-)>c(Na+)>c(CH3COOH) |
| D.等物质的量浓度CH3COOH溶液和CH3COONa溶液等体积混合,所得溶液中:c(CH3COOH)+2c(OH-)=2c(H+)+c(CH3COO-) |
以重晶石(主要成分为BaSO4)为主要原料制备立德粉(ZnS和BaSO4的混合物)的工艺流程如下: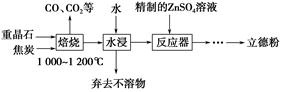
(1)焙烧时,焦炭需过量,其目的是:①____________________________;②____________________________。
(2)焙烧过程中发生的反应之一是4CO(g)+BaSO4(s) BaS(s)+4CO2(g),该反应的平衡常数的表达式为__________________________________________________。
BaS(s)+4CO2(g),该反应的平衡常数的表达式为__________________________________________________。
反应器中发生反应的化学方程式为____________________________________。
(4)用工业级氧化锌(含少量FeO和Fe2O3杂质)和硫酸制取硫酸锌溶液时,需先后加入H2O2溶液和碳酸锌精制,加入H2O2溶液时发生反应的离子方程式为
________________________________,加入碳酸锌的目的是将溶液中的Fe3+转化为红褐色沉淀,写出该反应的化学方程式:__________________________________________。
吡洛芬是一种用于治疗风湿病的药物。它的合成路线如下:

回答下列问题:
(1)B→C的反应类型为_____________________________。
(2)A→B反应的化学方程式为______________________________________
__________________________________。
从整个合成路线看,步骤A→B的目的是_______________________________。
(3)E的结构简式为____________________________。
(4)A在一定条件下可生成
F( )。写出同时满足下列条件的F的两种同分异构体的结构简式_____________________________。
)。写出同时满足下列条件的F的两种同分异构体的结构简式_____________________________。
①属于芳香族化合物;②是一种α氨基酸;③分子中有6种不同化学环境的氢。
(5)非那西汀是一种解热药,其结构简式为 ,写出以苯酚钠、CH3CH2OH和(CH3CO)2O为原料制备非那西汀的合成路线流程图(无机试剂任用) 。合成路线流程图示例如下:
,写出以苯酚钠、CH3CH2OH和(CH3CO)2O为原料制备非那西汀的合成路线流程图(无机试剂任用) 。合成路线流程图示例如下:
氟化铜是一种锂/氟化铜电池正极活性材料,可通过下列方法制备:在铂皿中将氧化铜用过量的40%氢氟酸溶解,先制成CuF2·5HF·5H2O,再将生成物放入镍管内的铂舟中,在干燥的氟化氢气流中以400%进行加热脱水,最后通入氮气。
(1)制备过程中用铂皿而不用玻璃器皿的原因是______________________________________(用化学方程式表示)。
(2) 锂/氟化铜电池放电时总反应为置换反应,其化学方程式为____________________________________________________。
(3)准备称取上述制备的样品(仅含CuF2和CuO) 2.120 g,在通风橱中加入稀硫酸至完全溶解,然后加入足量的氢氧化钠溶液,得沉淀,将沉淀充分灼烧,得1.680 g黑色固体,计算样品中CuF2和CuO的物质的量之比。
过硫酸钾( )具有强氧化性(常被还原为硫酸钾),80 ℃以上易发生分解。实验室模拟工业合成过硫酸钾的流程如下:
)具有强氧化性(常被还原为硫酸钾),80 ℃以上易发生分解。实验室模拟工业合成过硫酸钾的流程如下:
(1)硫酸铵和硫酸配制成电解液,以铂作电极进行电解,生成过硫酸铵溶液。写出电解时发生反应的离子方程式_____________________________________
___________________________________。
(2)已知相关物质的溶解度曲线如右图所示。在实验室中提纯过硫酸钾粗产品的实验具体操作依次为:将过硫酸钾粗产品溶于适量水中,________________,干燥。
(3)样品中过硫酸钾的含量可用碘量法进行测定。实验步骤如下:
步骤1:称取过硫酸钾样品0.300 0 g于碘量瓶中,加入30 mL水溶解。
步骤2:向溶液中加入4.00 0 g KI固体(略过量),摇匀,在暗处放置30 min。
步骤3:在碘量瓶中加入适量醋酸溶液酸化,以淀粉溶液作指示剂,用0.100 0 mol·L-1Na2S2O3标准溶液滴定至终点,共消耗Na2S2O3标准溶液21.00 mL。
(已知反应:I2+2S2O32-=2I-+S4O62-)
①若步骤2中未将碘量瓶“在暗处放置30 min”,立即进行步骤3,则测定的结果可能________(选填“偏大”、“偏小”、“无影响”);上述步骤3中滴定终点的现象是____________________________________________。
②根据上述步骤可计算出该样品中过硫酸钾的质量分数为_______________。
③为确保实验结果的准确性,你认为还需要____________________________。
(4)将0.40 mol过硫酸钾与0.20 mol硫酸配制成1 L溶液,在80 ℃条件下加热并在t时刻向溶液中滴加入少量FeCl3溶液,测定溶液中各成分的浓度如图所示(H+浓度未画出)。图中物质X的化学式为________________________。
能源的开发利用与人类社会的可持续发展息息相关。
Ⅰ.已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)
ΔH1=a kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH2=b kJ·mol-1
O2(g)=CO2(g) ΔH2=b kJ·mol-1
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH3=c kJ·mol-1
则C的燃烧热ΔH=________ kJ·mol-1。
Ⅱ.(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是________(填序号)。
A.C(s)+CO2(g)=2CO(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2H2O(l)=2H2(g)+O2(g)
D.2CO(g)+O2(g)=2CO2(g)
若以熔融的K2CO3与CO2为反应的环境,依据所选反应设计成一个原电池,请写出该原电池的负极反应:____________________________________________________________。
(2)某实验小组模拟工业合成氨反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,开始他们将N2和H2混合气体20 mol(体积比1∶1)充入5 L合成塔中,反应前压强为p0,反应过程中压强用p表示,反应过程中
2NH3(g) ΔH=-92.4 kJ·mol-1,开始他们将N2和H2混合气体20 mol(体积比1∶1)充入5 L合成塔中,反应前压强为p0,反应过程中压强用p表示,反应过程中 与时间t的关系如图所示。
与时间t的关系如图所示。
请回答下列问题:
①反应达平衡的标志是(填字母代号)________。
A.压强保持不变
B.气体密度保持不变
C.NH3的生成速率是N2的生成速率的2倍
②0~2 min内,以c(N2)变化表示的平均反应速率为________。
③欲提高N2的转化率,可采取的措施有________。
A.向体系中按体积比1∶1再充入N2和H2
B.分离出NH3
C.升高温度
D.充入氦气使压强增大
E.加入一定量的N2
(3)25 ℃时,BaCO3和BaSO4的溶度积常数分别是8×10-9和1×10-10,某含有BaCO3沉淀的悬浊液中,c(CO32-)=0.2 mol·L-1,如果加入等体积的Na2SO4溶液,若要产生BaSO4沉淀,加入Na2SO4溶液的物质的量浓度最小是________ mol·L-1。
卤素性质活泼,能形成卤化物、多卤化物等多种类型的化合物。
(1)卤化氢中,HF的沸点高于HCl,原因是____________________________
____________________________________________。
(2)如图为F-与Mg2+、K+形成的某种离子晶体的晶胞,其中“○”表示的离子是________(填离子符号)。
(3)多卤化物Rb[ICl2]分解时生成晶格能相对较大的铷(Rb)的卤化物,则该卤化物的化学式为_______________。
(4)BF3与NH3能发生反应生成X(H3BNF3),X的结构式为____________(用“→”表示出配位键):X中B原子的杂化方式为____________________________。
(5)有一类物质的性质与卤素类似,称为“拟卤素”[如(SCN)2、(CN)2等]。(CN)2的结构式为CNCN,该分子中σ键和π键数目之比为________。
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
| |
苯 |
溴 |
溴苯 |
| 密度/(g·cm-3) |
0.88 |
3.10 |
1.50 |
| 沸点/℃ |
80 |
59 |
156 |
| 水中溶解度 |
微溶 |
微溶 |
微溶 |

按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴液溴,有白雾产生,是因为生成了________气体。继续滴加至液溴滴完,装置d的作用是___________________________________________
_____________________________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑
②滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL水洗涤,NaOH溶液洗涤的作用是_____________________________________________________
___________________。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____________________________________________________________。
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中必须的是________(填入序号)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是________(填序号)。
A.25 mL B.50 Ml C.250 mL D.500 mL

 粤公网安备 44130202000953号
粤公网安备 44130202000953号