[广东]2012-2013年广东省珠海市高一上学期期末质检化学试卷(B)
下列事实与胶体性质无关的是
| A.在豆浆里加入盐卤做豆腐 |
| B.在河流入海处易形成沙洲 |
| C.一束平行光线照射蛋白质溶液时,从侧面可以看到一束光亮的通路 |
| D.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
Na2CO3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是
| A.Na2CO3是碱 | B.Na2CO3是盐 |
| C.Na2CO3是钠盐 | D.Na2CO3是碳酸盐 |
下列有关阿佛加德罗常数(NA)的说法错误的是
A.32克O2所含的原子数目为NA B.0.5 molH2O含有的原子数目为1.5 NA
C.1 molH2O含有的H2O分子数目为NA D.0.5 mol氯气含有的分子数目为0.5 NA
下列说法错误的是:
| A.钠在空气燃烧时先熔化,再燃烧,最后所得的产物是Na2O2 |
| B.铝因在空气中形成了一薄层致密的氧化膜,保护内层金属,故铝不需特殊保护 |
| C.铝制品在生活中非常普通,是因为铝非常不活泼 |
| D.铁因在潮湿的空气中形成的氧化物疏松,不能保护内层金属 |
将30 mL 0.5 mol·L-1 NaOH溶液加水稀释到500 mL,稀释后溶液中NaOH的物质的量浓度为
| A.0.3 mol·L-1 | B.0.03 mol·L-1 |
| C.0.05 mol·L-1 | D.0.04 mol·L-1 |
下列各组离子在无色溶液中能大量共存的是
| A.H+、Cl-、SO42-、K+ | B.K+、H+、Na+、HCO3- |
| C.Cu2+、K+、SO42-、Cl- | D.Ag+、NO3-、Cl-、K+ |
下列实验操作或事故的处理正确的是
| A.氢氧化钠固体放在小烧杯里称量 |
| B.金属钠着火燃烧时,可用水灭火 |
| C.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| D.观察钾元素焰色反应的操作是:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察。 |
用特殊方法把固体物质加工到纳米级(1nm-100nm)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子的大小和这种纳米粒子大小具有相同的数量级的是
| A.溶液 | B.悬浊液 | C.胶体 | D.乳浊液 |
下列溶液中,Cl-的物质的量浓度与50mL 1mol·L-1 AlCl3溶液中Cl-浓度相等的是 ( )
| A.150mL 1mol·L-1 NaCl溶液 | B.25mL 3mol·L-1 MgCl2溶液 |
| C.150mL 3mol·L-1 KClO3溶液 | D.75mL 1mol·L-1 FeCl3溶液 |
“神舟号”载人航天器中宇航员所在的轨道和返回仓都是密封的,宇航员吸入氧气、呼出二氧化碳,如果二氧化碳浓度过高,会使宇航员困乏,呼吸频率加快,严重的还会窒息,为解决此问题,应在航天仓中加入
| A.Na2O2 | B.Na2CO3 | C.NaOH | D.高压氧气瓶 |
配制一定体积、一定物质的量浓度的溶液,下列操作会使配得的溶液浓度偏小的是
| A.容量瓶中原有少量蒸馏水 |
| B.溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
| C.滴管加水时,有少量水滴到容量瓶外 |
| D.加水未达到刻度线 |
下列实验设计及其对应的离子方程式均正确的是
| A.用FeCl3溶液腐蚀铜线路板:Cu + Fe3+= Cu2+ +Fe2+ |
| B.Na与H2O反应制备H2:2Na+2H2O==2Na++2OH-+ H2↑ |
| C.用小苏打治疗胃酸过多:HCO3- + H+ ="=" CO2↑+ H2O |
| D.用食醋除去水瓶中的水垢: CO32- + 2H+ ="=" CO2↑+ H2O |
下列有关Na2CO3和NaHCO3性质的比较中,正确的是
| A.对热稳定性:Na2CO3 > NaHCO3 |
| B.常温时水溶性:Na2CO3 < NaHCO3 |
| C.与稀盐酸反应的快慢:Na2CO3 > NaHCO3 |
| D.水溶液的碱性:Na2CO3> NaHCO3 |
①现有下列物质:①盐酸 ② 纯碱③豆浆④烧碱⑤干冰⑥食盐水⑦氢气⑧泥水。
请根据它们所属的类别选择相应的序号填入下表中。
| 类别 |
单质 |
酸 |
碱 |
盐 |
氧化物 |
胶体 |
| 物质 |
|
|
|
|
|
|
(1)下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
|

①除去Ca(OH)2溶液中悬浮的CaCO3 ; ②从碘水中提取碘 ;
③用自来水制取蒸馏水 ; ④分离植物油和水 ;
⑤除去食盐水中的泥沙 ; ⑥与海水晒盐原理相符的是 。
(2)由可溶性铝盐制取氢氧化铝,需加入的试剂为: ;
离子方程式为: 。
白色的Fe(OH)2在空气中发生的颜色变化为 。
反应的化学方程式为: 。
实验室制配0.40mol/L的NaCl溶液80mL,有以下仪器:
①烧杯②100 mL量筒③100 mL容量瓶④500 mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)⑦药匙
(1)配制该溶液应选用___________mL容量瓶;
(2)向容量瓶中加入蒸馏水,到液面________________________时,改用___________加蒸馏水至液面最低点与刻度线相切,最后_________(填所选字母:A.左右旋转 B.上下颠倒)摇匀。
(3)取80ml配制好的溶液,加水稀释到200ml,这浓度变为 。
(4)配制一定物质的量浓度的溶液,造成浓度偏高的操作是
A.定容时,滴加蒸馏水超过刻度线
B.未洗涤烧杯和玻璃棒
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时,眼睛仰视刻度线
学生利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3·6H2O 晶体。(图中夹持及尾气处理装置均已略去)
(1)回答下列问题:所用铁粉中若有杂质,欲除去不纯铁粉中混有的铝粉可以选用的试剂为 (填序号)。
| A.稀盐酸 | B.氢氧化钠溶液 | C.浓硫酸 | D.FeCl3溶液 |
此步涉及反应的离子方程式为 。
(2)反应发生后装置B中发生反应的化学方程式是 。
D装置的作用: 。
(3)该小组学生把B中反应后的产物加入足量的盐酸,过滤,用上述滤液制取FeCl3·6H2O晶体,设计流程如下: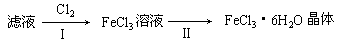
①用离子方程式表示步骤I中通入Cl2的作用 。
②为了检验某未知溶液是否是FeCl2溶液,同学们设计了以下实验方案加以证明。
向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液是FeCl2溶液。你认为此方案是否合理 (填“合理”或“不合理”)。





 粤公网安备 44130202000953号
粤公网安备 44130202000953号