[浙江]2011学年浙江省瑞安十校高二第二学期期中联考化学试卷
下列变化中不属于放热反应的是 ( )
| A.葡萄糖在人体内缓慢氧化 | B.灼热的炭和二氧化碳气体化合 |
| C.煤的燃烧 | D.过氧化钠与水的反应 |
下列说法正确的是( )
| A.凡是放热反应都是自发的 | B.铁在潮湿空气中生锈是自发过程 |
| C.自发反应都是熵增大的反应 | D.电解池的反应是属于自发反应 |
有关碰撞理论,下列说法中正确的是 ( )
| A.具有足够能量的分子(活化分子)相互碰撞就一定能发生化学反应 |
| B.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大 |
| C.升温能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 |
| D.催化剂不影响反应活化能,从而只影响反应速率不影响化学平衡 |
已知下列热化学方程式:Zn(s)+1/2O2(g)=ZnO(s)ΔH1="—351.1" kJ/mol
Hg(l)+1/2O2(g)=HgO(s) ΔH2="-90.7" kJ/mol 。
由此可知Zn(s)+HgO(s)=ZnO(s)+Hg(l)△H3。其中△H3的值是 ( )
| A.—441.8kJ/mol | B.—254.6kJ/mol | C.—438.9kJ/mol | D.—260.4kJ/mol |
在溶液中能共存,加OH-有沉淀析出,加H+ 能放出气体的是
| A. Na+、Cu2+、Cl-、SO42― | B.Ba2+、K+、OH-、NO3― |
| C. H+、Al3+、NH4+、CO32― | D.Na+、Ca2+、Cl-、HCO3― |
将0.1 mol下列物质置于1 L水中充分搅拌后,溶液中阴离子数最多的是 ( )
| A.KCl | B.Mg(OH)2 | C.Na2CO3 | D.MgSO4 |
下列各反应的化学方程式中,属于水解反应的是( )
A.H2O+ H2O  H3O++OH- H3O++OH- |
B.HCO3-+OH- H2O+CO32- H2O+CO32- |
C.CO2+H2O H2CO3 H2CO3 |
D.CO32-+H2O HCO3-+OH- HCO3-+OH- |
关于右图所示的原电池,下列说法正确的是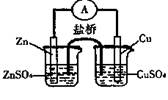
| A.电子从铜电极通过电流计流向锌电极 |
| B.盐桥中的阳离子向硫酸铜溶液中迁移 |
| C.锌电极发生还原反应,铜电极发生氧化反应 |
D.铜电极上发生的电极反应是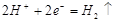 |
有两只串联的电解池(Pt为电极),甲池盛有足量的CuSO4溶液,乙池盛有足量的某硝酸盐的稀溶液。电解时当甲池电极析出6.4gCu时,乙池电极析出21.6g金属,则乙池的溶质可能是
| A.NaNO3 | B.Cu(NO3)2 | C.Al(NO3)3 | D.AgNO3 |
如图1所示,U形管中装入含有紫色石蕊的 试液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是:( )
试液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是:( )
| A.蓝、紫、红 |
| B.红、蓝、紫 |
| C.红、紫、蓝 |
| D.蓝、红、紫 |
有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为:C2++2e-→C,B—2e-→B2+则A、B、C、D金属性由强到弱的顺序为( )
A.A>B>C>D B.A>B>D>C C.D>A>B>C D.D>C>A>B
在不同情况下测得A(g)+3B(g)  2C(g)+2D(g)的下列反应速率,其中反应速率最大的是( )
2C(g)+2D(g)的下列反应速率,其中反应速率最大的是( )
A.υ(D)="0.4" mol·L-1·s-1 B.υ(C)="0.5" mol·L-1·s-1
C.υ(B)="0.6" mol·L-1·s-1 D.υ(A)="0.15" mol·L-1·s-1
在一定温度下,可逆反应X(g)+3Y(g) 2Z(g)已达到平衡的是
2Z(g)已达到平衡的是
| A.单位时间内消耗n mol X同时生成2n mol Z |
| B.单位时间生成a molX同时生成3a molY |
| C.X、Y、Z的浓度不再变化 |
| D.X、Y、Z的分子数之比为1∶3∶2 |
对于处于化学平衡状态的反应C(s) + H2O(g)  CO(g) + H2(g) △H>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是 ( )
CO(g) + H2(g) △H>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是 ( )
| A.增大C的量 | B.降低压强 | C.升温 | D.使用合适的催化剂 |
下列事实,能用勒夏特列原理解释的是( )
A.溴水中有平衡:Br2+ H2O  HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅 HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅 |
B.对CO(g) + NO2 (g) CO2 (g)+ NO(g) 平衡体系,增大压强可使颜色变深 CO2 (g)+ NO(g) 平衡体系,增大压强可使颜色变深 |
| C.工业上合成SO3,使用催化剂 |
| D.合成 NH3反应,在较高温度下进行 |
在一密闭容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器容积增加一倍,当达到新平衡时,B的浓度是原来的60%,则下列说法正确的是( )
bB(g)达平衡后,保持温度不变,将容器容积增加一倍,当达到新平衡时,B的浓度是原来的60%,则下列说法正确的是( )
| A.平衡向正反应方向移动 | B.物质A的转化率减小 |
| C.物质B的物质的量减少 | D.化学计量数a>b |
某温度下,在一容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
A.均减半 B.均加倍 C.均增加1mol D.均减少1mol
由一价离子组成的四种盐:AC、BD、AD、BC的1mol/L的溶液,在室温下前两种溶液的PH=7,第三种溶液的PH>7,最后一种溶液的PH<7,则( )
| |
A |
B |
C |
D |
| 碱性 |
AOH>BOH |
AOH<BOH |
AOH>BOH |
AOH<BOH |
| 酸性 |
HC>HD |
HC>HD |
HC<HD |
HC<HD |
相同温度、相同物质的量浓度的下列各组溶液,按pH值依次减小的顺序排列的是( )
| A.CH3COONa、Na2CO3、NaHSO4、NaCl | B.HCl、CH3COOH、NH4Cl、NaHCO3 |
| C.NaOH、Ba(OH)2、H2SO4、HCl | D.NH4Cl、CH3COOH、NaHSO4、H2SO4 |
下列实验操作完全正确的是( )
| 编号 |
实验 |
操作 |
| A |
钠与水反应 |
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B |
量取20.00ml KMnO4 溶液 |
用25ml碱式滴定管量取 |
| C |
排除碱式滴定管尖嘴部分的气泡 |
将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
| D |
取出分液漏斗中所需的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
含等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,设消耗CH3COOH溶液的体积依次为 ,则两者的关系正确的是( )
,则两者的关系正确的是( )
A. ; ; |
B. ; ; |
C. ; ; |
D. ; ; |
电解硫酸溶液时,放出25mL(标况)O2,若以等量的电量在同样条件下电解盐酸溶液,所放出的气体的体积最接近下列数据中的 ( )
| A.45mL | B.50mL | C.75mL | D.100mL |
(9分)(1)Na2CO3的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ; (2)氯化铝水溶液呈 性,原因是(用离子方程式表示):_____________________ 。
把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
有右图装置:回答下列问题: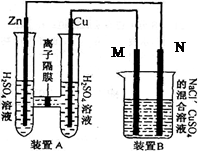
(1)装置A是_______池,B是_______池。
(2)装置A中的Zn极是_______极,
Cu极上的电极反应方程式为:__________________。
(3)装置B中是浓度均为1.0mol/L的NaCl、CuSO 混合溶液,溶液体积为500mL,M、N均为石墨电极,当装置A中Zn棒质量减少32.5g时,N上质量增加____________g;
混合溶液,溶液体积为500mL,M、N均为石墨电极,当装置A中Zn棒质量减少32.5g时,N上质量增加____________g;
(4)欲用装置B给用来给餐具镀银,N应该是 (填“银” 或“餐具”), 电镀液的主要成分是(填化学式) 。
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)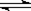 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是 。
a.容器中压强不变 b.混合气体中c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
用中和滴定法测定烧碱的纯度,若烧碱中含有少量不与酸作用的可溶性杂质,试根据实验回答:
(1)准确称取4.1g烧碱样品。
(2)将样品配成250mL待测液,需要的仪器有小烧杯、玻璃棒、 、胶头滴管。
(3)用 量取10mL待测液于 中(填仪器名称),并滴加几滴甲基橙作指示剂。
(4)用0.2010 mol·L-1标准盐酸滴定待测烧碱溶液,滴定时 手旋转 式滴定管的玻璃活塞, 手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色的变化,直到滴定终点,滴定终点时锥形瓶内溶液的PH约为 ,达到终点的具体现象是: 。
(5)若两次实验滴定的数据如下表:
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
10.00 |
0.50 |
20.4 |
| 第二次 |
10.00 |
4.00 |
24.1 |
据上表数据,计算待测烧碱溶液的浓度: 。
(6)根据上述各数据,计算烧碱的纯度:
(7)滴定时,滴定管尖嘴部分滴定前有气泡,滴定终了无气泡,测定结果将_______(填偏高、偏低或无影响,其它操作均正确)。
 2Z(g)
2Z(g) 。
。 aX(g)+3Y(g)的平衡常数。
aX(g)+3Y(g)的平衡常数。 粤公网安备 44130202000953号
粤公网安备 44130202000953号