2022年浙江省金华市中考化学试卷
科学以实验为基础,规范操作是科学实验取得成功的关键。下列实验操作规范的是( )
| A. |
|
B. |
|
| C. |
|
D. |
|
“宏观—微观—符号—量”是科学特有的表征物质及其变化的方法。2022年4月16日,神舟十三号载人飞船圆满完成飞行任务。火箭助推器使用偏二甲肼和四氧化二氮作为推进剂,燃烧时发生反应的微观示意图如图,下列说法不正确的是( )
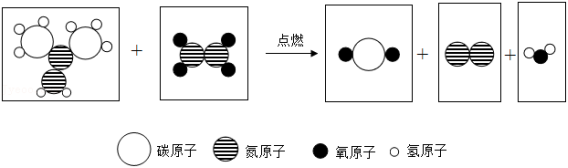
| A. |
从量的角度看:反应前后原子总数减少 |
| B. |
从微观构成看:氮气是由氮分子构成的 |
| C. |
从符号表征看:四氧化二氮的化学式是 |
| D. |
从宏观物质看:燃烧产物中含有单质与化合物两类物质 |
推理是根据已有的事实与结论推出新的判断的思维方法。下列根据已有事实或结论进行的推理正确的是( )
|
选项 |
事实或结论 |
推理或判断 |
|
A |
酸性溶液pH小于 7 |
pH小于7的溶液一定是酸性溶液 |
|
B |
碱能使无色酚酞溶液变红 |
能使无色酚酞溶液变红的一定是碱 |
|
C |
酸与碱反应生成盐和水 |
生成盐和水的反应一定是酸与碱的反应 |
|
D |
氧化物中都有氧元素 |
含有氧元素的化合物都是氧化物 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
如图曲线能正确反映下列化学变化中y与x变化关系的是( )

| A. |
锌粒中滴入稀硫酸:y代表氢气的质量 |
| B. |
溶液中通入 气体:y代表沉淀的质量 |
| C. |
氢氧化钠溶液中滴入稀盐酸:y代表混合溶液的pH |
| D. |
和 的混合溶液中加入 溶液:y代表沉淀的质量 |
性能神奇的金属钛( )是航空、军工、电力等领域的重要原材料。常温下钛不与非金属及强酸反应,加热时却可以和常见的非金属单质反应。金红石(主要成分 )是钛矿石之一,目前利用金红石大规模生产钛的过程是:
①在高温条件下在往金红石与碳粉混合物中通入氯气,反应制得四氯化钛( )和一种可燃性气体;
②在氩气的气流中,高温下用过量的镁跟四氯化钛反应制得钛和氯化镁。
完成下列问题:
(1)过程①中发生反应的化学方程式为 ;
(2)过程②中发生的反应,属于基本反应类型中的 。
学习《物质的溶解》时小科同学进行了如下实验:往A、B、C三只烧杯中分别装入等质量的水,在相同温度下,向三只烧杯中分别加入50g、25g、5g同种固体物质,充分溶解后,静置,现象如图所示。
回答下列问题:
(1)小科认为,A烧杯中的溶液一定是饱和溶液。他的判断依据是 ;
(2)A、B、C三只烧杯中,溶液的溶质质量分数大小关系是 。
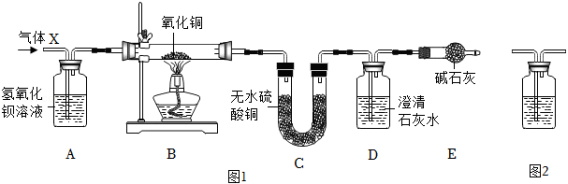
某混合气体X 由 、 、 (水蒸气)、 中的两种或两种以上组成, 气体依次通过如图1装置(假定每步反应均完全),现象分别为:A中溶液变浑浊;B中固体变为红色;C中粉末变为蓝色;D中溶液变浑浊。
完成下列问题:
(1)该实验能得出 气体一定存在的证据是 ;
(2)只要在图1中加装一个图2装置,就能确定原混合气体 中是否含有 。
①写出图2装置中试剂名称 ;
②该装置连接在图1中哪两个装置之间 (用字母表示)。
同学们在学习碱的化学性质时,进行了如图所示的实验。实验结束后,将A、B、C三个实验的废液倒入同一个干净烧杯D中,发现烧杯底部有白色沉淀,上层清液呈红色。

【提出问题】烧杯D中上层清液含有哪些溶质(除指示剂外)?
【分析讨论】小组讨论后认为,确定反应后物质成分的思维路径:①考虑反应物用量的不同;②抓住化学反应的本质,即微粒的重组。
某小组同学分析过程笔记如下:
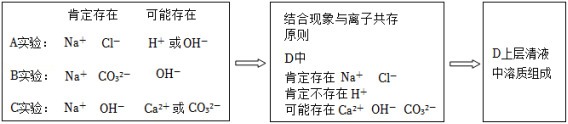
【初步结论】
(1)通过分析确定:烧杯D上层清液中肯定不含 ,肯定含有 、 。判断一定含有 、 。的依据是 ;
【实验探究】
小组按如下方案进行实验探究
|
实验 |
实验内容 |
实验现象 |
实验结论 |
|
Ⅰ |
取少量上层清液于试管中,加入过量碳酸钠溶液,静置 |
无沉淀,溶液呈红色 |
肯定没有 |
|
Ⅱ |
取少量上层清液于试管中,加入过量“?”溶液,静置 |
有白色沉淀,溶液呈红色 |
肯定有 、 |
(2)根据实验Ⅰ可以初步推断:上层清液中溶质(除指示剂外)所有可能的组成 (用化学式表示);
(3)实验Ⅱ中应加入过量的 溶液。
【实验结论】烧杯D中上层清液的溶质有指示剂、氯化钠、氢氧化钠、碳酸钠。
某校科学研究小组同学开展“二氧化碳的制取与性质”的实验探究。
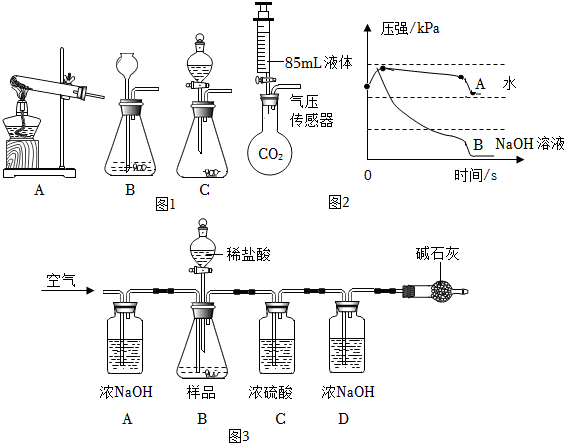
【实验原理】
【发生装置】
(1)结合实验原理,图1中发生装置可用于实验室制取 气体的是: (填字母)
【实验探究】
探究Ⅰ.影响因素探究
在制取 气体时,为了探究影响反应快慢的因素,小组同学进行了四组实验,如表所示
|
实验组别 |
甲 |
乙 |
丙 |
丁 |
|
大理石的质量/g、颗粒大小 |
m块状 |
m块状 |
m粉末状 |
m粉末状 |
|
盐酸的体积/mL、浓度 |
V稀盐酸 |
V浓盐酸 |
V稀盐酸 |
V浓盐酸 |
(2)若探究盐酸的浓度对上述反应的影响,可选择实验甲与 (选填实验组别)进行对照。
探究Ⅱ.性质探究
做 与 溶液发生反应的验证实验时,同学们将 溶液加入到充满 气体且质地较软的塑料瓶中,观察到塑料瓶变扁,由此得到 与 发生反应的结论。但有同学认为上述现象产生的原因还可能是 气体溶于水导致气压减小。
为回答该同学的质疑,小科进行了如下实验:在两个250mL的烧瓶中分别充满 气体,通过注射器同时向两个烧瓶中分别注入同体积的水和 溶液,最后得到烧瓶内压强与时间的关系曲线(如图2所示)。由此,小科得出 气体溶于水会导致塑料瓶变扁,同时 与 也发生了化学反应的结论。
(3)结合图2中A、B曲线变化特点,写出能证明 与 发生了化学反应的证据 。
【拓展提高】
小组同学完成某石灰石样品中 的质量分数测定,其方法是:将样品与一定量的稀盐酸反应,测定反应后生成的 质量,再根据 的质量求出样品中 的质量分数。
小组同学在实验室中组装了相应的实验装置(如图3)。小科利用该实验装置按如下步骤进行实验:
①先通一段时间的空气
②称量D装置的质量为
③打开分液漏斗的活塞,将稀盐酸全部加入锥形瓶,待充分反应后,关闭活塞
④再次通空气一段时间
⑤再次称量D装置的质量为
(4)有同学指出实验步骤③操作明显不合理,你认为该同学的理由是 。
为了保护生态环境,针对全球气候变化,中国政府向全球承诺,力争于2060年前实现“碳中和”。“碳中和”是指在一定时间内,使二氧化碳的排放总量与吸收总量平衡,实现“零排放”。实现“碳中和”通常可采取如下措施:
Ⅰ.碳减排:减少人类生产和生活中二氧化碳的排放量。
(1)下列做法不能实现“碳减排”的是 。
A.加高烟囱排放工业废气
B.推进新能源汽车使用
C.废弃物分类投放并回收利用
D.养成节约用水用电习惯
Ⅱ.碳吸收:①利用植物光合作用,这是自然界消耗二氧化碳的最重要途径;②利用“碳捕捉与封存技术”,即通过一定的方法,将工业生产中产生的 分离出来进行储存。在实际生产中,经常用 溶液来“捕捉” 流程如图所示(部分条件及物质未标出)。
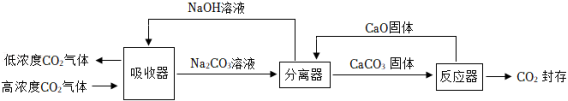
(2)用该技术进行“碳捕获”有效利用了原材料,该过程中被循环利用的物质有 。
(3)分离器中发生的反应:① ,② 。现有溶质质量分数为10.6%的 溶液100千克,求完全反应后,理论上可生成 的质量(要求根据化学方程式计算)。
Ⅲ.碳转化:指二氧化碳的资源化利用。
某项目学习小组用传感器开展“影响铁锈蚀因素”的探究,设计如图1所示实验装置并完成实验。实验过程中,传感器采集数据绘制得到如图2的甲、乙两幅曲线图。
【资料1】一定条件下,碳和氯化钠溶液可加快铁的锈蚀,但它们本身不参加反应。
【资料2】该实验步骤如下:
①检查装置气密性;
②装药品,将5克铁粉和2克碳粉加入锥形瓶,并加入2毫升饱和氯化钠溶液;
③立即塞紧橡皮塞,橡皮塞上已插有一支装有5毫升稀盐酸的注射器及传感器;
④观察现象,采集数据。
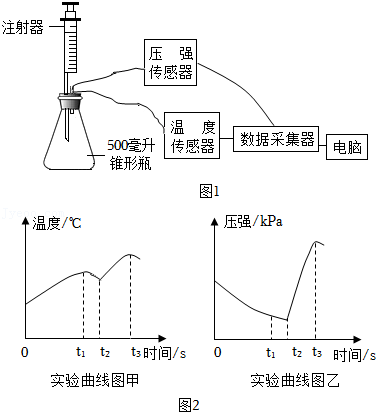
用所学知识及以上资料信息完成下列问题:
(1)实验进行一段时间后,注射器中的盐酸会自动注入瓶内,原因是 ;
(2)图2甲、乙曲线图中, 段温度升高,瓶内压强减小; 段温度升高,瓶内压强增大。解释产生这两个不同现象的原因。
 加热液体
加热液体 测溶液pH
测溶液pH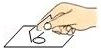 盖盖玻片
盖盖玻片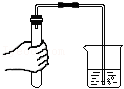 检查气密性
检查气密性 粤公网安备 44130202000953号
粤公网安备 44130202000953号