2020年辽宁省盘锦市中考化学试卷
下列有关燃烧与灭火的说法中,合理的是( )
A.燃烧一定伴随发光、放热现象
B.室内起火应迅速打开门窗通风
C.煤不完全燃烧有利于节约燃料
D.降低可燃物的着火点可以灭火
下列实验方案不能达到实验目的的是( )
选项 |
实验目的 |
实验方案 |
A |
探究水的组成 |
检验水通电分解后的气体产物 |
B |
探究分子运动 |
向水中加入少量品红,观察 |
C |
测定河水的酸碱度 |
取样,滴加无色酚酞溶液,观察 |
D |
区分蒸馏水和氯化钾溶液 |
取样,滴加少量硝酸银溶液,观察 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
化学是美好生活的创建者。
(1)人类目前使用的燃料大多来自化石燃料,其中比较清洁的是 。
(2)如图所示,活性炭的作用有 (填序号)。
①消毒
②过滤
③吸附
④降低硬度
(3)我国先进的5G通信设备使用了多种材料。聚氯乙烯塑料(PVC)用作天线罩,它属于 材料;高纯硅(Si)用作基带芯片,其制取原理:四氯化硅(SiCl 4)和氢气在高温条件下生成硅和氯化氢,写出该反应的化学方程式: 。

氧化汞粉末在加热条件下可生成汞和氧气。

根据所给信息,回答下列问题:
(1)该反应属于 (填基本反应类型)。
(2)氧化汞由大量的 (填"分子"或"原子")构成。
(3)请从微观角度描述该反应中氧气的形成过程: 。
化学研究物质的性质、结构及变化规律。
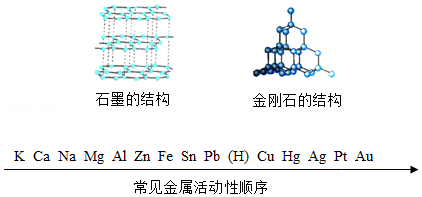
根据所给信息,回答下列问题:
(1)石墨可用作电极,是利用其具有良好的 。资料表明:石墨在一定条件下可以转化为金刚石,从结构上分析,这一转化中发生改变的是 。
(2)Na、Ag、Zn的金属活动性由强到弱的顺序是 。
(3)"真金不怕火炼"的化学原理: 。
(4)某化学小组设计的以下两个方案,均能除去铜屑中的少量铁屑。①加适量CuSO 4溶液,搅拌、过滤、洗涤;②加适量稀硫酸,搅拌、过滤、洗涤。请从中选出你认为最佳的方案,写出该方案中发生反应的化学方程式: ,简要评价该方案的优点: 。
化学实验是进行科学探究的重要方式。
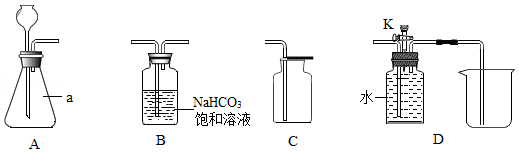
(说明:NaHCO 3饱和溶液的作用是吸收氯化氢气体;装置气密性良好;其他连接装置略)
实验一 氧气的实验室制取
(1)写出图中标号a仪器的名称: 。
(2)用A、C装置制取氧气,所需药品是 。
实验二:制取较纯净的CO 2并探究其性质
[药品准备]将30g质量分数为36%的浓盐酸稀释为9%的稀盐酸
(3)计算加入水的体积为 mL.(水的密度为1.0g/cm 3)
(4)配制稀盐酸时所需仪器有 (填序号)。
①量筒 ②玻璃棒 ③蒸发皿 ④胶头滴管 ⑤烧杯 ⑥托盘天平
[操作步骤]
步骤一:在A装置中加入足量石灰石,依次连接A、B、C装置,再向A中加入适量的稀盐酸。一段时间后,经检验A、B装置内的空气已排净。写出A中发生反应的化学方程式: 。
步骤二:待A中反应停止后,拆下C装置,再将D装置与A、B连接,关闭活塞K, (补全实验步骤),在D中收集实验所需的较纯净的CO 2。
步骤三:打开活塞K,用一支50mL注射器从D中缓慢抽取20mL CO 2,关闭K,再抽取20mL滴有紫色石蕊溶液的水溶液,用橡皮塞堵住注射器的针孔,轻轻振荡。观察到的现象: 。
[问题交流]步骤一中能充分证明A、B装置内的空气已排净的可靠方法是 。
[后续探究]……
某化学小组初步探究氢氧化钠的性质、变化和获得方法。
查阅相关资料:
Ⅰ.部分酸、碱和盐的溶解性表(室温)
阴离子/阳离子 |
OH ﹣ |
NO 3 ﹣ |
Cl ﹣ |
SO 4 2 ﹣ |
CO 3 2 ﹣ |
H + |
溶、挥 |
溶、挥 |
溶 |
溶、挥 |
|
K + |
★溶 |
溶 |
溶 |
溶 |
溶 |
Na + |
溶 |
溶 |
溶 |
溶 |
溶 |
Ca 2+ |
微 |
溶 |
溶 |
微 |
不 |
Cu 2+ |
不 |
溶 |
溶 |
溶 |
﹣﹣ |
说明:"溶"表示那种物质可溶于水,"不"表示不溶于水,"微"表示微溶于水,"挥"表示挥发性,"﹣"表示那种物质不存在或遇到水就分解了。
Ⅱ.氢氧化钠的工业制法:电解氯化钠饱和溶液
2NaCl+2H 2O 2NaOH+H 2↑+Cl 2↑
[性质与变化]
(1)上表★处"溶"对应的物质是 。
(2)完成下列物质转化,各写出一个符合要求的化学方程式。
①  。
。
②  。
。
[实践与应用]工业上常用电解氯化钠饱和溶液的方法生产氢氧化钠
(3)某化工厂计划生产16t氢氧化钠,请计算:
①氢氧化钠的相对分子质量是 。
②理论上需要氯化钠的质量是 t。
(4)工业生产中可制得含NaOH溶质质量分数约为45%的液碱产品,经进一步处理还可以制得固体氢氧化钠产品。请根据已有知识,对"进一步处理"中使用的方法提出设想并简要说明理由。
(5)工业固体氢氧化钠质量指标如图所示,请对产品中的杂质来源作出合理分析。
工业固体氢氧化钠质量指标 (合格品) 氢氧化钠(NaOH)/%≥98.0 碳酸钠(Na 2CO 3)/%≤1.0 氯化钠(NaCl)/%≤0.08 |
碳酸钠: 。
氯化钠: 。
 取用固体粉末B.
取用固体粉末B. 检查装置气密性
检查装置气密性 连接仪器D.
连接仪器D.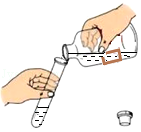 倾倒液体
倾倒液体 B.
B. C.
C. D.
D.
 粤公网安备 44130202000953号
粤公网安备 44130202000953号