2018年江苏省镇江市中考化学试卷
下列化学用语正确的是( )
| A. |
钙离子﹣﹣Ca +2 |
B. |
氯化钾﹣﹣KClO 3 |
| C. |
三个氢原子﹣﹣H 3 |
D. |
二氧化硅﹣﹣SiO 2 |
下列做法正确的是( )
| A. |
海鲜防腐,甲醛浸泡 |
B. |
回收塑料,再生减污 |
| C. |
煤气泄漏,明火检查 |
D. |
禁用农药,保护水源 |
下列归类不正确的是( )
选项 |
归类 |
内容 |
A |
化石燃料 |
煤、石油、天然气 |
B |
营养物质 |
糖类、油脂、蛋白质 |
C |
常见的碱 |
纯碱、苛性钠、氢氧化钾 |
D |
合成材料 |
涤纶、有机玻璃、合成橡胶 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
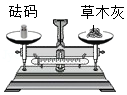
下图是粗略测定草木灰中碳酸钾含量的部分操作,其中对应操作不规范的是( )
| A. |
|
B. |
|
| C. |
|
D. |
|
下列实验方法正确的是( )
| A. |
用明矾对自来水进行杀菌消毒 |
B. |
用灼烧的方法区别羊毛线和棉纱线 |
| C. |
用点燃的方法除去CO 2中的CO |
D. |
用湿润的pH试纸测某溶液的pH |
下列排序正确的是( )
| A. |
利用金属的年代: |
| B. |
铁元素的质量分数: |
| C. |
碳元素的化合价: |
| D. |
物质在水中的溶解性: |
下列对实验现象的描述或实验操作正确的是( )
| A. |
镁条在空气中燃烧,有大量黑色固体生成 |
| B. |
为加快过滤速度,用玻璃棒搅拌滤纸上的悬浊液 |
| C. |
葡萄糖溶液与新制氢氧化铜混合加热至沸,出现红色沉淀 |
| D. |
配制一定体积的稀硫酸时,将水倒入盛有浓硫酸的量简中,并搅拌 |
如图是甲转化为丙的微观过程,下列说法不正确的是( )

| A. |
反应前后原子种类不变 |
B. |
转化①中甲和O 2反应的分子个数比为1:1 |
| C. |
转化②是化合反应 |
D. |
丙中氢、硫、氧元素的质量比为1:16:32 |
下列指定反应的化学方程式正确的是( )
| A. |
磷在氧气中燃烧:P+O 2 |
| B. |
小苏打受热分解:NaHCO 3 |
| C. |
不用铁桶配制波尔多液的原因:2Fe+3CuSO 4=Fe 2(SO 4) 3+3Cu |
| D. |
用食盐生产氯气和烧碱:2NaCl+2H 2O |
物质性质决定用途。下列说法不正确的是( )
| A. |
浓硫酸有吸水性,可用于干燥氨气 |
| B. |
洗洁精有乳化作用,可用于洗去碗筷上的油污 |
| C. |
氩气化学性质稳定,可用作焊接金属的保护气 |
| D. |
硫酸铜能使蛋白质变性,可用于游泳池水消毒 |
下列物质的转化在给定条件下均能实现的是( )
| A. |
H 2 |
| B. |
Ag |
| C. |
Ca(OH) 2溶液 |
| D. |
NaCl |
下列实验操作中不能达到实验目的是( )
选项 |
物质 |
目的 |
主要实验操作 |
A |
CO 2和SO 2 |
鉴别 |
分别通入稀KMnO 4溶液,观察现象 |
B |
CaO中含有CaCO 3 |
检验 |
取样,加入足量稀盐酸,观察现象 |
C |
MnO 2和KCl的混合物 |
分离 |
溶解、过滤,洗涤固体并烘干,蒸发滤液 |
D |
BaCl 2溶液混有Ba(NO 3) 2杂质 |
除杂 |
先加入过量Na 2SO 4溶液,过滤、洗涤;再向所得固体中加入适量稀盐酸 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
有Cu 2(OH) 2CO 3[M r=222]与Cu的混合物25.4g,在空气中加热一段时间,得剩余固体23.1g,向该固体中加入300.0g 9.8%的稀硫酸,固体完全溶解,测得反应过程中实际消耗9.8%的稀硫酸250.0g。下列说法正确的是( )
| A. |
剩余固体为纯净物 |
| B. |
上述加热过程中共生成H 2O和CO 2的质量为2.3g |
| C. |
原混合物中Cu 2(OH) 2CO 3与Cu的质量比为111:16 |
| D. |
最终所得溶液的质量为318.7g |
下列说法正确的是( )
| A. |
原子通过得失电子形成离子,离子一定不能形成原子 |
| B. |
不饱和溶液转化为饱和溶液,溶质的质量分数一定增大 |
| C. |
中和反应生成盐和水,有盐和水生成的反应一定是中和反应 |
| D. |
某溶液中滴入无色酚酞试液后变红,该溶液一定是碱性溶液 |
甲、乙试管中各盛有10.0g水,向其中一支试管中加入3.0gNa 2CO 3粉末,另一支试管中加入3.0g NaCl粉末,按图1、2进行实验,下列说法正确的是( )

| A. |
甲中加入的粉末是Na 2CO 3 |
| B. |
0℃时,甲中溶液一定不饱和,乙中溶液一定饱和 |
| C. |
Na 2CO 3中含有少量NaCl,可用冷却热饱和溶液的方法提纯Na 2CO 3 |
| D. |
30℃时,若使图1中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙中加入对应的溶质质量 |
烧杯中盛有MgSO 4和HCl的混合溶液100.0g,向其中逐滴滴加Ba(OH) 2溶液,产生沉淀的质量与滴加的溶液质量关系如图所示。下列说法正确的是( )

| A. |
a点对应溶液中只有1种溶质 |
B. |
b~c段只发生1个反应 |
| C. |
Ba(OH) 2溶液的溶质质量分数约为13.7% |
D. |
m=37.85 |
下列各组溶液,不用其他试剂就不能鉴别出来的是( )
| A. |
NaOH、KCl、稀HNO 3、CuSO 4 |
B. |
稀HCl、NaNO 3、K 2CO 3、Ca(NO 3) 2 |
| C. |
K 2SO 4、Ba(NO 3) 2、Na 2CO 3、NaCl |
D. |
BaCl 2、MgSO 4、稀HNO 3、NaOH |
如图是一种吸收废气中SO 2并得到H 2SO 4的方法,下列说法不正确的是( )

| A. |
电解过程中化学能转化为电能 |
| B. |
吸收时的反应为Na 2SO 3+SO 2+H 2O═2NaHSO 3 |
| C. |
阴极区产生的气体X是O 2 |
| D. |
该方法可减少酸雨的形成 |
用化学符号表示:
(1)金刚石 ;
(2)磁铁矿的主要成分 ;
(3)儿童缺少 元素严重时,会得侏儒症;
(4)相对分子质量最小的氧化物 。
选择下列适当的物质填空(选填序号):
A.干冰B.聚乙烯C.硝酸钾D.碳酸氢铵E.烧减F.活性炭G.熟石灰H.聚氯乙烯
(1)用于冰箱除异味的是 ;
(2)溶于水温度升高的是 ;
(3)可用于人工降雨的是 ;
(4)常用作复合肥料的是 ;
(5)可改良酸性土壤的是 ;
(6)可用于食品包装的是 。
如图,加热密封锤形玻璃泡内的碘颗粒,观察到玻璃泡内充满紫红色气体。
(1)该变化属于 变化(选填“物理”或“化学”);
(2)碘由固态变为气态时,分子间的空隙 (选填“变大”或“变小”)。

某兴趣小组利用实验室制CO2的废液得到CaCO3和NaCl晶体,过程如下:

(1)试剂X可用 (选填序号)。
a.NaOH溶液 b.Na2CO3溶液 c.K2CO3溶液
(2)操作I需要用到的玻璃仪器有 、 和烧杯。
(3)操作Ⅱ的名称为 。
将一定量的Na2O2固体投入到一定量的CuSO4溶液中,生成蓝色沉淀,同时产生一种能使带火星木条复燃的气体。
(1)写出该反应的化学方程式(其中Na2O2与CuSO4的化学计量数之比为1:1) 。
(2)实验结束后,某同学观察到蓝色沉淀中含有少量黑色的氧化铜,则上述反应是 (选填“吸热”或“放热”)反应。
请结合图回答问题:
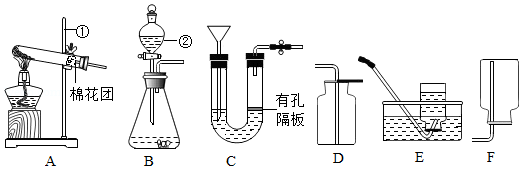
(1)仪器名称:① ,② 。
(2)用高锰酸钾制取氧气,可选用的发生装置是 (选填序号),该反应的化学方程式为 。用E装置收集氧气完毕后,应先 (选填"从水中取出导气管"或"熄灭酒精灯")。
(3)实验室制取CO 2,反应的化学方程式为 ,为方便控制反应的发生和停止,应选择的发生装置是 (选填序号),可用D装置收集CO 2的理由是 。
(4)NH 4Cl溶液与NaNO 2溶液混合共热可制取氮气,氮气和氢气在一定条件下可生成氨气。如图是实验室制氮气并模拟合成氨的装置。
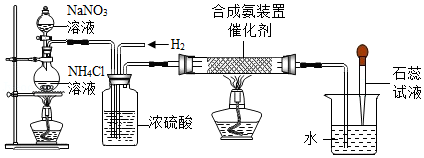
①合成氨时参加反应的氮气和氢气的质量比为 。
②实验中烧杯内导管口有气泡,还可观察到 现象。
如图为某同学所做的实验及现象。
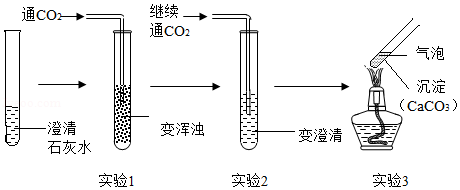
(1)实验1发生反应的化学方程式为 。
(2)实验2生成Ca(HCO 3) 2.实验3发生反应的化学方程式为 ,该实验说明CaCO 3比Ca(HCO 3) 2热稳定性 (选填"强"或"弱")。
(3)某地区硬水中溶有较多的可溶性Ca(HCO 3) 2、Mg(HCO 3) 2。
①生活中常用 来区分硬水和软水。
②煮沸硬水可降低水的硬度,同时生成难溶性混合物固体A。
【猜想】固体A中除CaCO 3外,还含有:
猜想1:只含MgCO 3
猜想2:只含Mg(OH) 2
猜想3:MgCO 3和Mg(OH) 2
【实验】取10.0g干燥的固体A,加入足量的稀盐酸充分反应,产生4.4gCO 2气体。
【结论】
①猜想1、2错误。其中判断猜想1错误的理由是 。
②猜想3正确,固体A中MgCO 3和Mg(OH) 2的质量比是 。
【拓展】在100℃时加热溶有较多Ca(HCO 3) 2、Mg(HCO 3) 2的硬水,1小时后得到CaCO 3和Mg(OH) 2•MgCO 3•3H 2O的固体混合物。写出Mg(OH) 2•MgCO 3•3H 2O与稀盐酸反应的化学方程式: 。
现有一包不纯的 Na2SO4固体,可能含有Fe(NO3)3、CaCO3、NaC1、MgCl2、Ba(OH)2中的一种或几种,现做如下实验:
(1)取少量固体溶于足量水,过滤得白色固体A和无色滤液B,则原固体一定不含 。
(2)取固体A,加入足量稀HCl,固体完全溶解,则原固体一定不含 ,一定含有 。
(3)取少量滤液B.滴加NaOH溶液,无明显现象,则原固体一定不含 。
(4)另取少量滤液B,先滴加过量 溶液,静置,再滴加AgNO3溶液,出现白色沉淀,则原固体还含有NaCl。
如图为某些物质间的转化关系,甲、乙、丙均为气体,乙有激性气味,丁是应用最广泛的金属。A是大理石的主要成分,G是一种化肥,H为红棕色固体。部分反应物和生成物已略去。
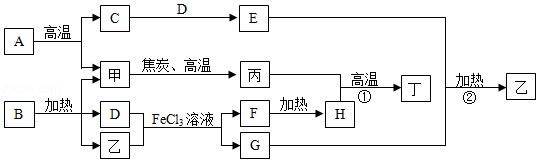
(1)化学式:B ,F 。
(2)自然界中,甲和D反应产生一种供给呼吸的气体,该反应名称为 。
(3)反应①、②的化学方程式:① ;② 。
(4)由反应②可知,在农业上施用G时应注意 。
铁及其化合物在生产生活中有广泛的应用。
(一)铁的应用和防护
(1)某麦片中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的铁元素,反应的化学方程式为 。
(2)铁锈主要成分是Fe 2O 3•nH 2O,铁生锈主要与空气中的 有关。
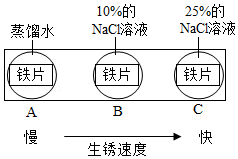
(3)如图实验说明NaCl在铁生锈中的作用是 。
(4)铁生锈的次要过程:Fe 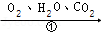 FeCO 3•nH 2O
FeCO 3•nH 2O  FeCO 3
FeCO 3
写出Fe转化为总反应的化学方程式 。
(5)为防止铁生锈,可对铁制品进行"发蓝"处理,使其表面生成致密氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为 。
(二)废铁的再利用
黄钠铁矾[NaFe x(SO 4) y(OH) z]是一种高效净水剂。用废铁屑(主要成分为Fe,含少量Fe 2O 3和FeCO 3)制备黄钠铁矾的主要流程如图:
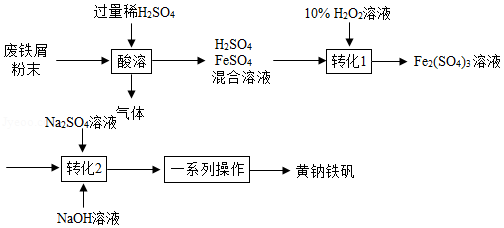
(1)将废铁屑研磨成粉末的目的是 。
(2)"酸溶"时H 2SO 4与Fe、FeCO 3反应,还发生反应的化学方程式有 和Fe+Fe 2(SO 4) 3=3FeSO 4。
(3)"转化1"发生反应的化学方程式为 。反应时温度不宜过高的原因是 。
(三)黄钠铁矾组成确定
称取9.70g黄钠铁矾,用如图装置进行热分解实验。
【资料】
①NaFe x(SO 4) y(OH) z在T 1℃分解会生成H 2O(气态),提高温度至T 2℃继续分解产生SO 3气体,并得到Fe 2O 3和Na 2SO 4。
②浓硫酸可用于吸收SO 3。
(1)装配好实验装置后,先要 。
(2)分别控制温度在T 1℃、T 2℃对A中固体加热。
①控制温度在T 1℃加热,实验后测得B装置质量增加1.08g。
②用D装置替换B装置,控制温度在T 2℃,加热至反应完全。
③T 1℃、T 2℃时,加热后均通入一段时间N 2,目的是 。
(3)反应完全后,将A装置中固体溶于足量水,过滤、洗涤、烘干得4.80g固体,将滤液蒸干得1.42g固体(不含结晶水)。
结论:NaFe x(SO 4) y(OH) z中,x:y:z= 。
反思:若该实验过程中缺少C装置,则x:z的值 (选填"偏大""偏小"或"不变")。
 称量
称量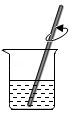 溶解
溶解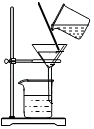 过滤
过滤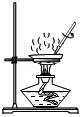 蒸发
蒸发



 P 2O 5
P 2O 5 NaOH+CO 2↑
NaOH+CO 2↑ Cl 2↑十2NaOH+H 2↑
Cl 2↑十2NaOH+H 2↑ H 2O
H 2O  H 2CO 3
H 2CO 3 AgCl
AgCl  AgNO 3溶液
AgNO 3溶液 CaCO 3
CaCO 3 NaHCO 3
NaHCO 3  Na 2SO 4溶液
Na 2SO 4溶液 粤公网安备 44130202000953号
粤公网安备 44130202000953号