2017年湖北省黄冈市中考化学试卷
分类是化学学习和研究的重要方法之一,下列分类中不正确的是( )
A.纯净物:氧气、干冰、水银
B.肥料:二氧化碳、硫酸铵、硝酸钾
C.单质:金刚石、铁粉、黄铜
D.盐:氯化钠、硝酸钠、碳酸钙
下列说法:①煤中含有硫和氮元素,燃烧会产生SO2和NO2等污染物,大量排放到空气中能形成酸雨。②烟草燃烧释放的物质中,尼古丁能与血红蛋白结合而引起中毒。③自来水收费项目中收取水资源费和水处理费是不合理的。④洗涤剂具有乳化作用能去除油污。⑤米和面中含有的糖类物质主要是淀粉,它在人体的消化系统中经淀粉酶的催化作用,最终变为葡萄糖。⑥硝酸铵(NH4NO3)能促进植物茎、叶生长茂盛。⑦亚硝酸盐是有毒的物质,不能作为食品添加剂使用。⑧房间里着火应立即打开门窗。正确的是( )
A.①②③④⑥B.④⑤⑥⑦⑧C.①④⑤⑥⑦D.②③⑤⑦⑧
对于下列化学用语,有关说法正确的是( )
①NO2 ②Fe2+ ③K2MnO4④ ⑤
⑤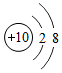
A.①表示的是两种元素组成的化合物
B.③中锰元素的化合价为+7
C.②和⑤均表示阳离子
D.④和⑤表示的微粒化学性质相同
下列关于化学反应2X=2Y+3Z的说法,错误的是( )
A.该反应一定是分解反应
B.在反应中,X、Y、Z三种物质的粒子数目比为2:2:3
C.该反应可能有单质生成
D.若反应生成了a gY和b gZ,则消耗X的质量一定大于(a+b)g
在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
物质 |
甲 |
乙 |
丙 |
丁 |
反应前质量/g |
35.0 |
24.6 |
16.8 |
26.6 |
反应后质量/g |
X(未知) |
49.0 |
0 |
53.0 |
下列说法中,不正确的是( )
A.反应后物质甲的质量为1.0 g
B.反应中甲、丙的质量比为5:4
C.乙是生成物
D.该反应可能是置换反应
Si是重要的半导体材料,半导体工业中有一句行话“从沙滩到用户”,指的是利用沙子(主要成分SiO2)制取高纯度的Si.已知硅与碳有相似的化学性质,SiHCl3(三氯氢硅)能与水反应,其工艺流程和主要化学反应如图:

①2C+SiO2 Si(不纯)+2CO↑
Si(不纯)+2CO↑
②3HCl+Si(不纯)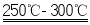 SiHCl3+H2
SiHCl3+H2
③SiHCl3+H2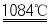 3HCl+Si(高纯)
3HCl+Si(高纯)
下列说法不正确的是( )
A.①的目的是将二氧化硅转化为单质硅
B.物质A可循环利用
C.整个制备过程必须达到无水无氧
D.反应③中SiHCl3是还原剂
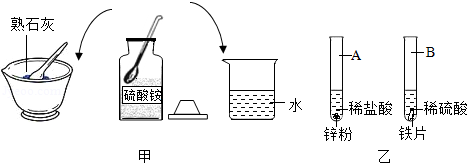
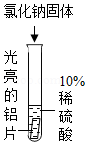
化学是以实验为基础的学科,根据实验甲、实验乙回答下列问题:
(1)甲实验验证了硫酸铵的物理性质是 (答一条即可);化学性质是 。
(2)乙实验是金属与酸反应的实验,实验过程中可观察到A试管中的现象是 ,B中铁片反应后溶液呈 色。
请用所学化学知识回答下列问题。
(1)根据海水晒盐原理,析出晶体后的溶液是氯化钠的 溶液。
(2)厕所用清洁剂损坏大理石地面 。(用化学方程式表示)。
(3)CO是大气污染物之一。用氯化钯(PdCl2)可以监测微量CO的存在。把含有CO的混合气通入到PdCl2溶液中时,得到了金属钯、氯化氢和二氧化碳,通过测定金属钯的质量,即可计算出CO的质量,从而测定处大气中CO的含量。 试写出该反应的化学方程式 (用化学方程式表示)。
化学就在我们身边,化学与生产生活息息相关。请回答下列问题:
(1)人类社会的生活和发展离不开常见金属和金属材料。用我们学到的化学知识和方法能分析和解释许多现象。
①下列生活用品,主要利用金属具有良好导热性的是

②下列事实不能用金属活动性顺序解释的
A.铝制品抗腐蚀能力比铁制品强 B.铜能将银从硝酸银溶液中置换出来
C.不能用金属铜与稀硫酸反应制取氢气 D.铁的硬度比铜大
(2)氧气是一种化学性质比较活泼的气体,在点燃和加热的条件下能与许多物质发生化学反应。试回答下列与氧气有关的问题:
①空气中氧气的体积分数约占 。
②如图是一些物质与氧气反应的实验,甲中物质安静燃烧时火焰的颜色是 。任选一个实验,写出一个化学反应的方程式 。
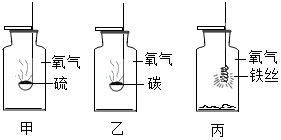
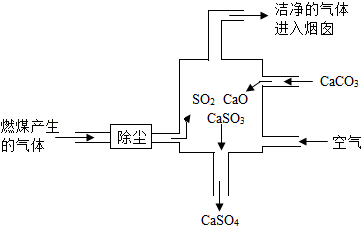
③如图是某燃煤发电厂处理废气的装置示意图,其工艺原理是:向废气处理塔中投入CaCO 3和鼓入空气在高温条件下,将SO 2全部吸收。
(Ⅰ)废气处理塔中发生的反应可用一个总化学方程式表示,写出这个反应的化学方程式: 。
(Ⅱ)若该发电厂每天有16kg二氧化硫产生,则投入的CaCO 3的质量至少是 kg。
有A、B、C、D、E五种物质,如图所示,(“→”表示某一种物质经一步反应可转化为另一种物质,“﹣﹣”表示相连两物种物质能发生化学反应,部分反应物、生成物已略去)。已知A、B、C含有相同的金属元素,D与C发生中和反应,D与BaCl2溶液混合,无任何现象,E是相对分子质量最小的氧化物。回答下列问题。
(1)E的化学式为: 。
(2)C的化学式为: 。
(3)B与D反应: (用化学方程式表示)。

根据如图回答问题。

(1)仪器①的名称是 。
(2)实验室用氯酸钾制取氧气的化学方程式为 。所选用的收集装置是E或 (填字母序号,下同)。
(3)实验室用大理石和稀盐酸制取二氧化碳,所选用的发生装置是 。收集一瓶二氧化碳,将燃着的木条放在瓶口,若观察到 ,说明瓶中已充满二氧化碳。
(4)某同学用较浓的盐酸制取氢气,若要制取并收集一瓶较纯净的氢气,则装制连接顺序序号为 。
(5)实验室制取2g氢气,理论上应取锌的质量是 g。
铝是重要的轻金属,广泛应用于航空、电讯和建筑领域。铝亦有其特殊的性质,试根据以下信息填空或简答。
(1)按金属的活动性顺序,铝比锌 。但是将铝片和锌粒分别投入稀硫酸中,铝片表面产生的气泡却比锌粒少而慢。为了探究铝与酸反应的规律,小强用相同质量、相同形状的光亮铝片设计如下实验。
实验一 |
实验二 |
实验三 |
实验四 |
|
实验现象 |
铝表面产生气泡很小且慢 |
铝表面产生大量气泡 |
铝表面产生大量气泡 |
铝表面产生大量气泡且快 |
(2)比较实验三、实验四说明铝与酸反应产生氢气的速率,与 有关。
(3)比较实验一、实验二说明铝与酸反应产生氢气的速率,可能与 、 粒子和温度、金属与酸的接触面积等多种因素有关。
(4)写出实验二中发生反应的化学方程式 。
(5)小芳将长条状铝片的一端放在酒精灯火焰上灼烧片刻,轻轻摇动铝条,受热一段会左右摇晃,却不像蜡烛那样滴落。为探究其原因,小芳查阅资料得知:铝的熔、沸点分别是660℃、2460℃;氧化铝的熔、沸点分别为2054℃、2980℃。
试解释上述实验现象: 。
 测定溶液的pHB.
测定溶液的pHB.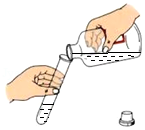 倾倒溶液
倾倒溶液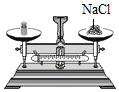 称量固体D.
称量固体D. 取用固体粉末
取用固体粉末


 粤公网安备 44130202000953号
粤公网安备 44130202000953号