浙江省温州市六校九年级上学期期中联考科学试卷
植物分类的依据很多,根据有无种子这一特征,下列植物中,与其它植物不属同一类别的是( )

| A.蕨类 | B.海带 | C.葫芦藓 | D.水稻 |
下列各组物质中,俗名、化学名称和化学式表示的不是同一种物质的是( )
| A.熟石灰、氢氧化钙、Ca(OH)2 |
| B.烧碱、碳酸钠、Na2CO3 |
| C.盐酸、氯化氢水溶液、HCl |
| D.食盐、氯化钠、NaCl |
铝镁合金是新型建筑装潢材料,主要用于制作窗框、卷帘门、防护栏等。下列性质与这些用途无关的是( )
| A.不易生锈 | B.密度小 | C.导电性好 | D.强度高 |
生活中废弃的铝质易拉罐、破铁锅、废铜线等可归为一类加以回收,它们属于( )
| A.有机物 | B.金属或合金 | C.氧化物 | D.非金属 |
古代“银针验毒”的原理是:4Ag+2H2S+O2═2X+2H2O,X的化学式为( )
| A.AgS | B.Ag2O | C.Ag2S | D.Ag2O2 |
硫酸的工业用途广泛,如生产染料、农药、化学纤维、塑料等。实验室也可以用稀硫酸来制取H 2S气体:FeS + H2SO4= FeSO4 + H2S↑,该反应属于( )
| A.分解反应 | B.化合反应 | C.置换反应 | D.复分解反应 |
在烧杯中分别盛放相等质量的下列物质,暴露在空气中一段时间后,质量增加、溶质质量分数减小的是( )
| A.浓盐酸 | B.浓硫酸 | C.氯化钠溶液 | D.浓硝酸 |
在下图四支试管中,分别加入2ml质量分数相同的盐酸溶液,再分别加入质量、表面积均相等的Mg、Cu、Zn、Fe,立即把四个相同的气球分别套在各试管口上。其中气球不会发生膨胀的是( )
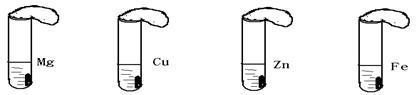
A B C D
如图甲是一物体在100牛顿的拉力作用下升高l米;乙是另一物体在100牛顿平行斜面的拉力作用下沿斜面移动1米;丙是又一物体在100牛顿水平拉力作用下沿水平方向移动了1米。则( )
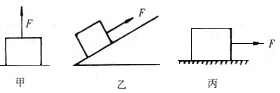
| A.甲图中的拉力做功最多 |
| B.乙图中的拉力做功最多 |
| C.丙图中的拉力做功最多 |
| D.三种情况做的功一样多 |
2013年5月,某市发生了一起亚硝酸钠中毒事件。亚硝酸钠外观酷似食盐,有咸味,加热会分解,放出有臭味的气体。请结合下表信息,判断以下区别亚硝酸钠和氯化钠的方法错误的是( )
| |
亚硝酸钠(NaNO2) |
氯化钠(NaCl) |
| 跟稀盐酸作用 |
放出红棕色的气体 |
无反应 |
| 跟硝酸银溶液作用 |
生成浅黄色沉淀 |
生成白色沉淀 |
A.滴加稀盐酸 B.加热
C.品尝味道 D.滴加硝酸银溶液
学习了功率的知识后,小科和几位同学准备做“比一比谁的功率大”的活动。以下是他们设计的三套方案,其中可行的是( )
①测量出各自的体重、爬楼用的时间和爬楼的高度,算出功率进行比较。
②控制爬楼的时间相同,测量出各自的体重、爬上楼的高度,算出功率进行比较。
③控制爬楼的高度相同,测量出各自的体重、爬楼用的时间,算出功率进行比较。
| A.只有② | B.只有②③ | C.只有①③ | D.①②③ |
除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
| 选项 |
物质 |
杂质 |
除杂所用的试剂和方法 |
| A |
CaO固体 |
CaCO3固体 |
加入适量的稀盐酸 |
| B |
NaOH溶液 |
Ca(OH)2溶液 |
先加入过量的Na2CO3溶液,再过滤 |
| C |
CO2气体 |
CO气体 |
点燃 |
| D |
H2气体 |
HCl气体 |
先通过NaOH溶液,再通过浓硫酸 |
自来水生产中常通入适量氯气进行杀菌消毒,氯气与水反应如:Cl2+H20=HCl+HClO,市场上有一些不法商贩为牟取暴利,用自来水冒充纯净水(蒸馏水)出售。你能用来鉴别纯净水真伪的试剂是( )
| A.酚酞试液 | B.稀硫酸 | C.硝酸银溶液 | D.氢氧化钠溶液 |
推理是学习科学的一种重要方法,不合理的推理会得出错误的结论。以下推理正确的是( )
| A.碱溶液的pH都大于7,pH大于7的溶液不一定是碱溶液 |
| B.溶液是均一、稳定的混合物,均一、稳定的物质一定是溶液 |
| C.原子可以构成物质,物质一定是由原子构成 |
| D.有些金属和稀硫酸反应放出气体,与稀硫酸反应放出气体的物质一定是金属 |
有关显微镜的操作步骤有:①转动细准焦螺旋、②转动粗准焦螺旋、③转动物镜转换器、④调节光圈、⑤移动装片。如图是在显微镜下观察到的草履虫,要将甲图转换成乙图,下列操作顺序中哪个是正确的?( )
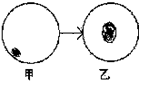
| A.⑤③④②① | B.②③①④ |
| C.⑤④③① | D.⑤③④① |
如图所示,条形磁铁置于水平桌面上,电磁铁的右端固定,闭合开关,当滑动变阻器滑片P向右移动时,条形磁铁仍保持静止,在此过程中,条形磁铁受到的摩擦力的方向和大小是( )
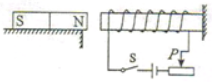
| A.方向向左,逐渐增大 | B.方向向右,逐渐增大 |
| C.方向向左,逐渐减小 | D.方向向右,逐渐减小 |
把铁粉和氧化铜的混合物加入到一定量的盐酸中,充分反应后过滤。在滤液中加入少量铁粉,无现象。下列判断正确的是( )
| A.滤渣中一定不含铜 |
| B.滤渣可能是铜和铁的混合物 |
| C.滤液中含有FeCl2和HCl |
| D.滤液中含有FeCl2和CuCl2 |
如图,小球从左端由静止释放,在左右摆动过程中,不计空气阻力与摩擦,则( )
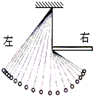
| A.小球到达最右侧时动能最大 |
| B.到达右侧最高点时动能不为零 |
| C.左侧最高点的高度大于右侧最高点的高度 |
| D.左侧最高点的高度等于右侧最高点的高度 |
芋艿是一种常见的食品,既可以当粮食,又可作蔬菜。
(1)新鲜芋艿在去皮时会产生一种白色的汁液,汁液内含有一种碱性物质——皂角甙,沾上他会奇痒难忍。下列物质可用来涂抹止痒的是 。
A.食醋 B.熟石灰 C.纯碱
(2)有经验的人遇到这种情况,会将手靠近火源烘一烘,也可以达到止痒的效果;如果将带皮芋艿煮熟后,再用手去皮也不再会有痒的感觉。根据上述现象,请你推测皂角甙的一种化学性质: 。
一氧化碳气体在生产生活中有着广泛的应用。请回答下列问题:
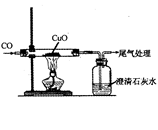
(1)物质的性质决定其用途。因为一氧化碳具有 性,所以可用作燃料。
(2)如图是一氧化碳还原氧化铜的实验。请指出实验中能证明发生了化学变化的证据 (写一条)。
2013年6月11日17时37分59秒,神舟十号飞船顺利升空。

(1)6月13日13时18分,天宫一号目标飞行器与神舟十号飞船成功实现自动交会对接。宇航员们将进入天宫一号并开展实验,由于航天员长期处于失重环境下生活会出现肌肉萎缩、骨丢失等症状,需要通过相关锻炼进行维护。“天宫一号”中搭载有太空锻炼器材,其中 不能作为失重防护锻炼器材(选填“拉力器”或“哑铃”)。

(2)航天员王亚平于6月20日上午10:04-10:55进行太空授课,地面现场有两三名热心提问的中学生,与300多公里之外的“太空老师”进行互动,只见王亚平拿出一个装有水的饮水袋,慢慢的倒过来,结果水并没有流出来,原因是太空中没有 。
火星的自转轴倾角与地球相近,公转一周约为地球公转时间的两倍,火星大气以二氧化碳为主。2012年8月,美国“好奇”号火星车成功着陆火星表面,开展对火星奥秘的探索。
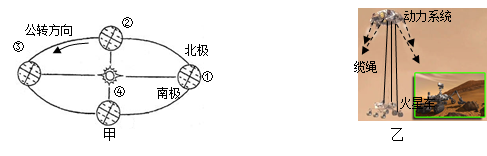
(1)火星有时被称为“红色行星”,是因为火星地表富含氧化铁(Fe2O3),已知氧元素的化合价为-2价,则铁元素的化合价为 。
(2)火星也有与地球类似的季节变化,当火星位于图甲中的③位置时,此时火星北半球的季节类似于地球北半球的 季。
(3)由于物体间力的作用是 的,着陆时,火箭动力系统沿图乙中箭头所指方向喷气,就可以获得缓慢地盘旋下降所需的阻力。
(4)相同物体在火星表面受到的重力相当于地球表面的五分之二。着陆后,缆绳自动切断,“好奇”号火星车与动力系统完全分离,静止在火星表面的火星车受到的重力 (选填“大于”、“等于”或“小于”)火星表面对火星车的支持力。
今年4月25日,台州市某废金属收购场发生火灾,十几吨金属镁爆燃,八辆装满清水的消防车却没有用武之地,最后用十三吨沙土才将大火扑灭。
(1)此场合不能用水灭火,因为金属镁在高温条件下会跟水反应生成氢氧化镁和氢气,请写出该反应的化学方程式 ;
(2)沙土灭火的原理是使可燃物 ;
(3)火灾现场的另一种金属A却没有发生燃烧,但其表面变黑。由此判断:镁的金属活动性 A的金属活动性。(选填“>”、“=”或“<”)
无明显现象的化学反应可通过滴加其它试剂的方法,使之产生明显现象以证明反应确实发生了。例如以下三个实验:

(1)当观察到实验甲中出现 时(填实验现象),说明NaOH与HCl恰好完全反应。
(2)乙和丙中哪一实验与甲类似,也是通过反应前后溶液颜色的改变来证明反应发生的? 。
将科学知识系统化,有助于对问题的认识。
(1)根据物质的组成和性质可对无机化合物进行分类。请在Na、H、O、S四种元素中选择几种元素按要求组成一种物质,将其化学式填在下面③的横线上。

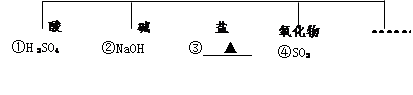
(2)概念之间、化学反应之间具有包含、并列、交叉等关系。左下图表示其中某一关系,下表中甲、乙符合下图所示关系的是 (选填下列表中选项)。
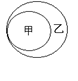
| |
A |
B |
C |
D |
| 甲 |
两栖类 |
光合作用 |
中和反应 |
化合反应 |
| 乙 |
脊椎动物 |
呼吸作用 |
复分解反应 |
氧化反应 |
向下图所示的烧杯中逐滴加入Ba(OH)2溶液,直到恰好完全反应后静置片刻,塑料小方块处于漂浮状态。(塑料小方块不与溶液反应)
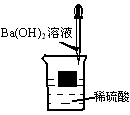
(1)在滴加Ba(OH)2溶液的过程中,塑料小方块受到的浮力将 。(选填“变大”、“变小”或“不变”)
(2)与滴加Ba(OH)2溶液之前相比,塑料小方块浸入液体中的体积 (选填“变大”、“变小”或“不变”),原因是 。
氮化铝(AlN)是一种新型材料。某氮化铝样品中含有碳或氧化铝杂质。已知氮化铝和NaOH溶液能反应,其反应方程式为①AlN+NaOH+H2O=NaAlO2+NH3↑② 氧化铝也能与氢氧化钠溶液反应而全部溶解,但不生成气体。现用如图所示中的一些装置来进行相关实验。根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)。
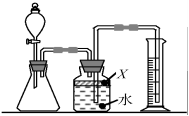
(1)实验操作为:
a.往锥形瓶中放入适量的AlN 样品;
b.打开分液漏斗的活塞往锥形瓶中加入过量的浓NaOH;
c.检验装置气密性;
d.测定收集到水的体积。
正确的操作顺序为 ( 用a、b、c、d 字母表示)。
(2)广口瓶中的试剂X 宜选用 (填写序号)。
| A.稀硫酸 | B.酒精 | C.植物油 | D.水 |
(3)若广口瓶内的液体没有装满(上方留有少量空间),则实验测得NH3体积将 (选填“偏大”、“偏小”或“无影响”)
在“探究一定电压下,电流与电阻的关系”的实验中,老师提供的实验器材有:电源(电压恒为4.5Ⅴ),电流表、电压表各一个,开关一个,四个定值电阻(5Ω、10Ω、15Ω、20Ω),三只滑动变阻器(规格分别为“20Ω 2A”、“50Ω 1A” 、“100Ω 1A”),导线若干。
(1)请根据图甲的电路图用笔画线将图乙实物图连接完整。
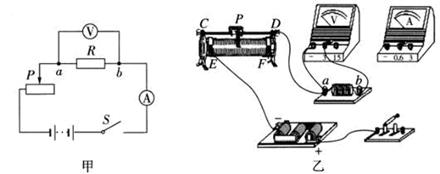
(2)小柯开始实验,一闭合开关,发现电压表指针满偏(示数达到3V),其原因可能是 。
(3)小柯实验时,在a、b间先接入5Ω的电阻,闭合开关,移动滑片P,使电压表的示数为1.5Ⅴ,并记下相应的电流值;再改接10Ω的电阻,此时滑片P应向 (选填“E”或“F”)端移动.
(4)小柯为完成用四个定值电阻进行实验,他应选择的滑动变阻器规格是 。
某校科学兴趣小组的同学用纯锌粒与稀盐酸反应制氢气时,发现产生气泡的速度较慢。就采用补加浓度更大的盐酸来提高反应速度,但不小心误加了CuSO4溶液,结果产生气泡的速度也大大加快,于是他们对此问题进行实验探究。
[提出问题]:此反应速度明显加快的原因是什么?
[作出猜想]:①加入的CuSO4溶液中的SO42-使反应速度加快
②加入的CuSO4溶液中的H2O使反应速度加快
③加入的CuSO4溶液中的Cu2+ 使反应速度加快
④加入CuSO4溶液后,锌置换出的少量铜使反应速度加快
你认为最不可能的猜想是 (填序号)。
[实验验证]:用a、b、c、d四支干净试管取等质量且过量的纯锌粒后,再分别向试管中加入同体积同溶质质量分数的稀盐酸。
请完成下表:
| 实验步骤 |
实验主要现象 |
实验结论 |
| 1.向a试管中加入少量NaCl晶体 |
产生气泡速度不变 |
钠离子对反应速度无影响 |
| 2.向b试管中加入少量 晶体 |
产生气泡速度不变 |
猜想①不成立 |
| 3.向c试管中加入少量Cu粉 |
产生气泡速度明显加快 |
猜想④成立 |
| 4.向d试管中加入少量CuSO4粉末 |
产生气泡速度,与第3步c试管的速度几乎一样快 |
猜想③成立 |
[得出结论]:在锌和稀盐酸反应时,加入 ,可加快化学反应速度。
某兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。请你与他们一起完成以下探究活动:
【对固体猜想】
猜想I: 全部是NaOH
猜想Ⅱ:全部是Na2CO3
猜想Ⅲ:部分是NaOH,部分是Na2CO3。
【实验和推断】
| 实验步骤 |
实验现象 |
| ①取少量白色固体于试管中,加水至全部溶解。 |
无色溶液 |
| ②向溶液中滴加适量物质X的溶液。 |
现象A |
| ③再向试管中滴加几滴酚酞试液。 |
现象B |
(1)若现象A为有气泡产生,则加入的X溶液是 ,说明氢氧化钠已经变质。
(2)若X是Ca(OH)2溶液,现象A有白色沉淀,现象B为无色酚酞试液变红色,该实验 (填“能”或“不能”)说明样品中有NaOH,原因 。
(3)若猜想Ⅲ成立,则X是 溶液。
【反思应用】
(4)保存NaOH溶液的方法是 。
实验室里常用锌和稀硫酸反应来制取氢气。林辉同学取6.5g的锌并加入50g一定质量分数的硫酸溶液,恰好完全反应后,得到56.3g硫酸锌溶液。发生反应的化学方程式是:Zn+H2SO4=ZnSO4+H2↑. 请你计算:
(1)生成氢气的质量为 g.
(2)硫酸溶液中溶质的质量分数。
公交公司最近更换了一批新型混合动力公交车,在进行新车测试时获得一些数据:新型公交车总质量为4×103kg,轮胎与地面总接触面积为0.4m2,车匀速行驶时所受阻力是车总重的0.5倍,公交车在牵引力作用下在平直公路上匀速行驶,2min内行驶了1200m(取g=10N/kg,忽略司机的质量).求:
(1)新型公交车静止时对水平地面的压强是多少?
(2)2min内牵引力所做功是多少?功率是多少?
为防止酒驾事故的出现,酒精测试仪被广泛应用。有一种由酒精气体传感器制成的呼气酒精测试仪,当接触到的酒精气体浓度增加时,其电阻值降低,如图甲所示。当酒精气体的浓度为0时,R1的电阻为60Ω。在图乙所示的工作电路中,电源电压恒为8V,定值电阻R2=20Ω。求: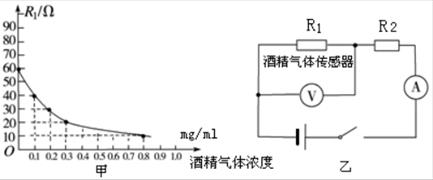
(1)当被检测者的酒精气体的浓度为0时,电压表的示数是多少;
(2)现在国际公认的酒驾标准是0.2mg/ml≤酒精气体浓度≤0.8mg/ml,当电流表的示数为0.2A时,试通过计算判断被检测者是否酒驾。
如图是某同学在厨房里看到的食用纯碱(主要成分是Na2CO3)包装袋信息,他带了一包食用纯碱到学校实验室。

(1)为测定室温下Na2CO3的溶解度,在编号为A、B、C、D的四个烧杯中各加入室温下的水100g,并分别加入取自实验室的Na2CO3固体,搅拌至充分溶解。实验数据记录如下表:
| 烧杯编号 |
A |
B |
C |
D |
| 水的质量(g) |
100 |
100 |
100 |
100 |
| 碳酸钠的质量(g) |
30 |
35 |
40 |
50 |
| 溶液的质量(g) |
130 |
135 |
140 |
140 |
分析上述数据可知,烧杯编号是 中的溶液是饱和溶液。室温下,Na2CO3的溶解度是 克。
(2)为确定食用纯碱的纯度,称取自带的食用纯碱5.4 g,放入烧杯中,再滴加盐酸至刚好完全反应,共用去稀盐酸25 g,得溶液质量为28.2g(反应的化学方程式为:2HCl+Na2CO3 = 2NaCl+H2O+CO2↑,杂质溶于水且与盐酸不反应)。通过计算判断纯碱样品中碳酸钠的质量分数是否与包装信息相符。(计算结果精确到0.1%)

 粤公网安备 44130202000953号
粤公网安备 44130202000953号