2011年全国统一高考理综试卷(福建卷)化学部分
下列关于化学与生产、生活的认识不正确的是
| A. | 等均是造成温室效应的气体 |
| B. | 使用清洁能源是防止酸雨发生的重要措施之一 |
| C. | 节能减排符合低碳经济的要求 |
| D. | 合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |
依据元素周期表示元素周期律,下列推断正确的是
| A. | 的酸性比 的强 |
| B. | 的碱性比 的强 |
| C. | 的热稳定性依次增强 |
| D. | 若 和 的核外电子层结构相同,则原子序数: |
下列关于有机化合物的认识不正确的是
常温下0.1醋酸溶液的 ,下列能使溶液的措施是
| A. | 将溶液稀释到原体积的10倍 | B. | 加入适量的醋酸钠固体 |
| C. | 加入等体积0.2 盐酸 | D. | 提高溶液的温度 |
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是
25℃时,在含有、的某溶液中,加入过量金属锡(),发生反应:,体系中()和()变化关系如右图所示。下列判断正确的是

I.磷、硫元素的单质和化合物应用广泛。
(1)磷元素的原子结构示意图是
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500°C生成白磷,反应为:
每生成 1时,就有
(3)硫代硫酸钠()是常用的还原剂。在维生素C(化学式)的水溶液中加入过量溶液,使维生素 完全氧化,剩余的用溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
在一定体积的某维生素C溶液中加入溶液,充分反应后,用溶液滴定剩余的,消耗 溶液.该溶液中维生素C的物质量是
(4)在酸性溶液中,碘酸钠()和亚硫酸钠可发生如下反映:
生成的碘可以用淀粉液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
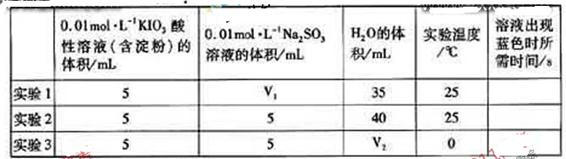
该实验的目的是
II稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(5)钵(Ce)是地壳中含量最高的稀土元素,在加热条件下易发生水解,无水,可用加热和固体混合物的方法来制备。其中,的作用是
(6)在某强酸性混合稀土溶液中加入,调节 ≈3. 通过下列反应形成Ce
(OH)4沉淀得以分离。完成反应的离子方程式:
四氧化钛()是制取航天航空工业材料--钛合金的重要原料。由钛铁矿(主要成为是)制备等产品的一种工艺流程示意如下:

回答下列问题
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
(无色)+=(紫色)+
(紫色)+(无色)+
加入铁屑的作用是
(2)在②→③工艺过程中需要控制条件以形成溶胶,该溶胶的分散质颗粒直径大小在
(3)若把③中制得的固体用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉。已知25 ℃时,,该温度下反应的平衡常数K=
(4)已知:
写出④中和焦炭、氯气反应生成液态和气体的热化学方程式:
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4,可采用
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水充足搅拌、过滤。
(1)往滤渣中加入过量 溶液,过滤。氢氧化铝与溶液反应的离子方程式是。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察的现象是。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定中生成的沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌、中的反应物外,还有:
(4)中反应生成的化学方程式是。
(5)下列各项措施中,不能提高测定准确度的是(填标号)。
a.在加入盐酸之前,应排净装置内的气体
b.滴加盐酸不宜过快
c.在之间增添盛有浓硫酸的洗气装置
d.在之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00样品三份,进行三次测定,测得平均质量为3.94。则样品中碳酸钙的质量分数为_。
(7)有人认为不必测定中生成的质量,只要测定装置在吸收前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是
氮元素可以形成多种化合物。
回答以下问题:
(1)基态氮原子的价电子排布式是。
(2)、、三种元素第一电离能从大到小的顺许昌是。
(3)肼()分子可视为分子中的一个氢原子被-(氨基)取代形成的另一种氮化物。
①分子的空间构型是;分子中氮原子轨道的杂化类型是。
②肼可用作火箭燃料,燃烧时发生的反应是:
若该反应中有4 键断裂,则形成的键有。
③肼能与硫酸反应生成。晶体类型与硫酸铵相同,则的晶体内不存在(填标号)
| A. |
a.离子键 b.共价键 c.配位键 d.范德华力 |
(4)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体得4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物是别的是(填标号)。

a. b. c. d.
透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶。制备它的一种配方中含有下列四种物质

填写下列空白:(1)甲中不含氧原子的官能团是;下列试剂能与甲反应而褪色的是(填标号)
a. 溶液 b.石蕊溶液 c.酸性溶液
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:
(3)淀粉通过下列转化可以得到乙(其中A-D均为有机物):

的分子式是,试剂可以是。
(4)已知:
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是。
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110。丁与溶液作用显现特征颜色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号