河北省邯郸市高三第二次模拟考试(理综)化学部分
生活中常用到一些化学知识, 下列分析中正确的是
下列分析中正确的是
| A.变质的植物油有难闻的特殊气味,是山于植物油发生了水解反应 |
| B.某雨水样品放置一段时间后pH由4.68变为4.00,是因为水中溶解的CO2增多 |
| C.氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性 |
| D.加碘食盐中添加碘酸钾而不用碘化钾,是因为碘酸钾能溶于水而碘化钾不溶于水 |
下列说法正确的是
| A.形成离子键的叨阳离了•间只存在静电吸引力 |
| B.HF、HCl, HBr, HI的热稳定性和还原性从左到右依次减弱 |
| C.第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| D.元素周期律是元素原子核外电子排布周期性变化的结果 |
下列现象或反应的原理解释正确的是
| |
现象或反应 |
原理解释 I |
| A |
铝箔在酒精灯 火焰上加热熔化但不滴落 火焰上加热熔化但不滴落 |
铝箔表面生成的氧化物炅有高熔点 |
| B |
钠和氧气在加热条件下进行反应 |
该反应为吸热反应 |
| C |
碳酸钠和氢氧化钠溶液中滴加酚酞,溶液都呈红色 |
碳酸钠和氢氧化钠都玷碱 |
| D |
将CH3CH2Br与NaOH溶液混合加热,再滴加AgNO3溶液,未产生浅黄色沉淀 |
CH3CH2Br未发生水鮮 |
下列装置或操 作能达到实验目的的是
作能达到实验目的的是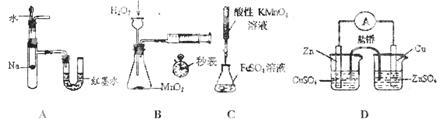
| A.验证反应的热效应 | B.定量测定化学反应速率 |
| C.滴定FeSO4溶液 | D.构成铜锌原电池 |
下列说法正确的是
A. 的结构中含有酯基 的结构中含有酯基 |
| B.乙醇、乙酸、乙酸乙酯都可以与NaOH溶液反应 |
| C.1mol葡萄糖可水解生成2 mol乳酸(C3H6O3) |
| D.油脂和蛋白质都是能发生水解反应的高分子化合物 |
下列离子方程式不正确的是
A.用惰性电极电解氯化钠溶液: |
B.向FeBr2溶液中通入Cl2,使溶液中一半的Br-被氧化: |
C.用双氧水和稀硫酸处理印刷电路板: |
| D.向碳酸氢钙溶液中加入足量的氢氧化钠溶液: |

 燃料电池(DBFC)的结构如右图,有关该电池的说法正确的是
燃料电池(DBFC)的结构如右图,有关该电池的说法正确的是
A. 电极B为负极
B. 电池负极区的电极反应为:
C. 放电过程中,Na+从正极区向负极区迁移
D. 在电池反应中,每消耗1 L 6moH.L-1 H2O2溶液,理论上流过电路中的电子为6NA
. 已知:还原性 ,氧化性
,氧化性 。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法正确的是
。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法正确的是
| A.反应过程中的氧化产物均为SO3 |
| B.a点时剩余NaIISO3的物质的量为1.2 mol |
| C.b点时的还原产物可能是KI或NaI |
| D.当溶液中r与I2的物质的量之比为1:1时,加入的KIO3为1.1 mol |
现代工业将煤炭气化,既可以提高燃料的利用率、减少CO、SO2,等的排放,又可以扩大水煤气的广泛用途
(1) 已知:
则反应 =_______,(用含
=_______,(用含 的代数式表示)
的代数式表示)
(2) CO和H2在一定条件下合成甲醇的反应为: ΔH3。向容积均为1L的a, b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2
ΔH3。向容积均为1L的a, b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2 的混合气体,控温,进行实验,测得相关数据如下图1和图2。
的混合气体,控温,进行实验,测得相关数据如下图1和图2。
①该反应的 _______O (选填“<”、“>”或“=”)。
_______O (选填“<”、“>”或“=”)。
②对图2进行分析,从a到c段曲线变化特点看,温度升高甲醇体积分数增高的原因可能是:______________将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有_______
(3)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态K2CO3为电解质。写出该燃料电池负极的电极反应式_______。
某强酸性溶液X,含有
 中的一种或几种离子,取溶液进行连续实验,能实现如下转化:
中的一种或几种离子,取溶液进行连续实验,能实现如下转化:
依据以上信息,回答下列问题:
(1)上述离子中,溶液X中肯定含有的是: ____________________________不能肯定的是_____________________.对不能确定是否存在的离子,可以另取X溶液于一支试管中,选择下列试剂中的一种加入X溶液中 根据现象就可判般,则该试剂最好是:______________①NaOH溶液,②酚酞试剂,③石蕊试剂,④pH试纸⑤KSCN溶液,⑥KMnO4溶液。
根据现象就可判般,则该试剂最好是:______________①NaOH溶液,②酚酞试剂,③石蕊试剂,④pH试纸⑤KSCN溶液,⑥KMnO4溶液。
(2 )气体F的化学式为:______________,沉淀K的化学式为:_______,实验中,可以观察到反应②的现象是____________________________.
(3) 写出步骤①所有发生反应的离子方程式_____________________________ ;
(4) 要使步骤③中,D、H2O,O2三种物质恰好发生化合反应,则D、H2O, O2物质的量之比是____________________________。
室温下,将一定浓度的Na2CO3溶液滴入CnSO4溶液中得到了蓝色沉淀。为了确定沉淀的组成,某研究性学习小组进行了以下试验和研究。
(一)【提出假说】
假设一:两者反应只生成CuCO3—种沉淀;
假设二:这两者祁互促进水解,生成Cu(OH)2—种沉淀,则此反应化学方程式为:____________________________;
假设三:生成的是CuCO3和Cu(OH)2两种沉淀。
(二)【理论探究】
查阅资料:CuCO3, Cu(OH)2均不带结晶水;
Cu(OH)2均不带结晶水;
 ;若由此数据判断,假设_______是不正确的。
;若由此数据判断,假设_______是不正确的。
(三)[实验探究]
步滋一:将CuCO4溶液倒入等浓度等体积的Na2CO3溶液中并搅拌,有蓝色沉淀生成。
步骤二:将沉淀从溶液中分离出来,其操作方法为:①过滤,②_______,③干燥。
步骤三:利用下图所示装置,进行定量分析:
①仪器组装好后首先要进行的实验操作是_____________________。
②实验结束时通入过量空气的作用是_____________________。
③数据记录和分析:实验过程中测定的数据有:W1——样品的质量;W2——反应后装置B中残渣的质量;W3——反应生成的水的质量;W4——反应后生成二氧化碳的质量,为了测定其组成,至少需要其中 个数据,请将可能的组合填入下表中(每个空格中填一种组合,有几种组合就填几种,不必填满.)
下图中A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3(发生反应,C和D的相对分子质量相等,且E为无支链的化合物。
根据上图回答问题:
(l) C分子中的官能团名称是_______;化合物B不_发生的反应是_______(填字母序号):
a、加成反应b、取代反应C、消去反应d、酯化反应e、水解反应f、置换反应
(2) 反应②的化学方程式是______________。
(3) 试分析反应②加热的原因。
I、___________________________________。
II 、___________________________________
(4) A的结构简式是_____________________。
(5) 同时符合下列三个条件的B的同分异构体的数目有_______个。
I.间二取代苯环结构;II.属于非芳香酸酯;III-与FeCl3溶液发生显色反应。
写出其中任意一个同分异构体的结构简式_____________________。
(6) 常温下,将C溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
从m组情况分析,所得混合溶液中由水电离出的c(OH )=_______mol.L-1.
n组混合溶液中离子浓度由大到小的顺序是______________。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号