福建省福州市八县(市)高三上学期期中联考化学卷
化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是( )
| A.北京奥运会燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
| B.太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 |
| C.加热能杀死甲型H1N1流感病毒是因为病毒的蛋白质受热变性 |
| D.废旧电池应集中回收,并填埋处理 |
下列过程中,不涉及化学变化的是( )
| A.用明矾净化水 |
B.烹鱼时加入少量的料酒和食醋可减少腥味,增加香味 |
| C.焰色反应 |
| D.烧菜用过的铁锅,经放置常出现红棕色斑迹 |
若 代表阿伏加德罗常数,下列说法正确的是 ( )
代表阿伏加德罗常数,下列说法正确的是 ( )
A.1 molCl2参加反应转移电子数一定为2 |
B.将31g的 溶解于1L水中,所得溶液中 溶解于1L水中,所得溶液中 的物质的量浓度为1 mol/L 的物质的量浓度为1 mol/L |
| C.常温常压下,22.4L的NH3和16g CH4中所含有的电子数都是10NA |
D. |
Al2O3、MgO和SiO2都可以制耐火材料,其原因是 ( )
| A.Al2O3、MgO和SiO2都是不溶于水的固体 |
| B.Al2O3、MgO和SiO2都是属于离子晶体 |
| C.Al2O3、MgO和SiO2都是氧化物 |
| D.Al2O3、MgO和SiO2都有很高的熔点 |
下列离子方程式书写可能正确的是 ( )
A.钠与水的反应:Na + H2O === Na+ +OH-+ H2↑  |
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| C.在氢氧化钠溶液中通入少量的CO2:2OH- + CO2=CO32- + H2O |
| D.在硫酸铝溶液中加入过量氨水:Al3+ + 4OH- = AlO2-+2H2O |
在下述条件下,一定能大量共存的离子组是 ( )
| A.强酸性溶液中:Al3+、K+、Mg2+、Cl-、SO42- |
| B.PH=13的溶液中:Cl-,HCO3-,NO3-,NH4+ |
| C.c(Fe3+)="0.1" mol·L-1的溶液中:Na+、SCN—、Cl-、Br- |
| D.强碱性溶液中:ClO-、SO42-、SO32-、Na+ |
下列关于可逆反应:2SO2 + O2 2SO3的说法正确的是( )
2SO3的说法正确的是( )
| A.1mol SO2与足量O2反应,可以生成1mol SO3 |
| B.平衡时,c(SO2)∶c(O2)∶c(SO3)=2∶1∶2 |
| C.当O2的质量不再变化时,反应达到平衡 |
| D.当反应达到平衡状态时,v(O2)=0 |
将足量Na2O2 投入FeCl2 溶液中, 可观察到的现象是( )
①生成白色沉淀 ②生成红褐色沉淀 ③有气泡产生 ④反应后溶液变无色。
| A.①④ | B.②③④ |
| C.①③ | D.① |
根据反应(1)Br2 +2Fe2+=2Br-+2Fe3+ ; (2)2Fe3+ + 2I-= 2Fe2+ + 2I2 ,可判断离子的还原性由强到弱的顺序正确的是 ( )
| A. Br- > Fe2+ >I- | B.Fe2+>I-> Br-_ |
| C.Br->I-> Fe2+ | D.I-> Fe2+ > Br- |
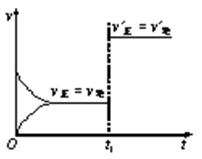
对可逆反应:2A(g) + B(s)  3C(s) + 2D(g);ΔH﹤0 下图所示为正逆反应速率(v)与时间(t)关系的示意图,
3C(s) + 2D(g);ΔH﹤0 下图所示为正逆反应速率(v)与时间(t)关系的示意图, 如果在t1时刻改变以下条件:①升温; ②加入催化剂;
如果在t1时刻改变以下条件:①升温; ②加入催化剂; ③加入A;④加压;⑤减少C,
③加入A;④加压;⑤减少C,
符合图示的条件是 ( )
| A.②④ | B.①② |
| C.③④ | D.④⑤ |
短周期元素X,Y,Z、W在周期表中的位置如右图所示,则下列说法中错误的是
A.X,Y,Z中X的单质最稳定 |
B.W的最高价氧化物对应的水化物的化学式为HWO4 |
C.Y能溶于水生成HYO和HY |
| D.能发生Cl2 + H2Z="===Z" + 2HCl的反应 |
关于下图所示的原电池,下列说法正确的是 ( )
| A.电子从铜电极通过检流计流向锌电极 |
| B.盐桥中的阳离子向硫酸铜溶液中迁移 |
| C.锌电极发生还原反应,铜电极发生氧化反应 |
D.铜电极上发生的电极反应是 |
下图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触,而稀硫酸准备的又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )
①食盐水 ②KNO3溶液
③适量硫酸铜稀溶液 ④Na2CO3溶液
⑤CCl4 ⑥浓氨水
| A.①③⑤ | B.②⑥ |
| C.③⑤ | D.①②④ |
在Fe2(SO4)3溶液中,加入ag铜,完全溶解后,再加一定量的铁粉,充分反应后有残余固体,将残余固体加入到稀H2SO4中,有气泡产生,则下列说法正确的是( )
| A.残余固体一定没有铜 |
| B.残余固体中含有铁和铜 |
| C.最后得到的溶液中一定含有Cu2+ |
| D.最后得到的溶液中加入KSCN溶液一定会变血红色 |
把Ba(OH)2溶液滴入明矾溶液中,当SO42-全部转化成BaSO4沉淀,此时溶液中铝元素的主要存在形式是( )
| A.Al3+ | B.Al(OH)3 | C.AlO2— | D.Al3+和Al(OH)3 |
(1)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃10kPa下,10g甲醇燃烧生成CO2和液态水时放热226.8kJ。请写出表示甲醇燃烧的热化学方程式:
(2) 某些化学反应可用下式表示:A + B 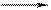 C + D + H2O
C + D + H2O
请回答下列问题:
①若A、D均可用于消毒,且C是家家户户的厨房必备的调味品之一,写出该反应的离子方程式 。
②若A为水垢的主要成分之一,B是日常生活常见有机物(厨房用品),
写出该反应的化学方程式: 。
③若C、D均为气体且都能使澄清石灰水变浑浊,则只用
或 (任写两种试剂的名称)就可以鉴别C、D两种气体。
A、B、C、D、E、F为短周期主族元素,原子序数依次增大,A原子中不含中子; C、D同周期;D的质子数 比B与C的最外层电子数之和少1,D的最外层电子数是次外层电子数的3倍;E与A同族,F与E同周期并且是该周期原子半径最小的金属元素。
⑴由A、B元素组成的是石油化工生产标志的物质的结构式是:
⑵由A、D、E元素组成的物质与A、D、F元素组成的物质反应的离子方程式是:__________
⑶B、C、D分别与A组成最简单化合物的稳定性从大到小顺序是:
⑷由A、C、D元素组成盐含有的化学键有 (填化学键类型)该物质与A、D、E元素组成的物质反应的方程式是:
⑸E、F所在的金属元素最高价氧化物对应水化物的碱性由弱到强顺序是 (用化学式表示)
一般测定样品中成分含量的实验应重复2—3次。为了测定某氢氧化钠固体中混有的碳酸钠的质量分数,甲、乙、丙三位同学分别设计了如下实验方案:
Ⅰ.甲同学的方案如上图所示:
(1)根据甲同学的实验装置图分析,在每次实验过程中所进行的称量操作至少要进行 次;如何来检验A装置的气密性?
。
(2)甲同学重复进行了三次实验,得到碳酸钠的质量分数的数据存在较大的偏差,你认为可能引起测量结果偏低的原因是 (填序号)。
A.装置内原有空气中的二氧化碳气体也被碱石灰吸收;
B.装置外空气中的水蒸气和二氧化碳被碱石灰吸收;
C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收;
D.加入稀硫酸的量不足反应不充分
(3)为了让甲的实验测量结果更准确,在其他实验步骤都正确下,你认为图中的实验装置应该如何改进实验装置:
Ⅱ.乙同学的方案是:从下图所提供的装置中选择实验装置,代替甲同学实验的B、C,通过测定放出的二氧化碳的体积(不考虑二氧化碳溶于水)来计算。
选择最简装置的连接顺序为 ;
Ⅲ.丙同学的方案是:称取样品m g,并溶解,加入过量氯化钡溶液,过滤、洗涤、烘干、称量,得固体n g。
(1)配制100 mL 0.10 mol·L-1 BaCl2溶液及过滤实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外还有_______________________________(填仪器名称);
(2)混合物中碳酸钠的质量分数为(用m、n表示) 。
(3)Ca2+、Ba2+都可以使CO32-沉淀完全。能否使用氯化钙溶液代替氯化钡溶液?为什么?
实现化学实验绿色化的要求,有效地减少污染,可把化学实验设计成微型化。某研究性学习小组的学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即用表面皿盖好。
(1)在a处观察到的实验现象:_____________________________________。
在c处观察到的实验现象:______________________________________。
(2)e处反应的离子方程式为___________________________________。
该反应中氧化剂和还原剂的物质的量之比为__________________________。
(3) d处反应所产生的现象为___ _______________。
标准状况下,当有0.112 L Cl2被NaOH溶液吸收后,转移电子为________mol。
(4)通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?________(填“能”或“不能”),若能,其氧化性由强到弱的顺序是____________ ___。
海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:
(1)实验操作①的名称是 ;实验操作③的名称是 、 ,所用主要仪器名称为 。
(2)提取碘的过程中,可供选择的有机试剂是 (填序号)。
A.酒精(沸点78℃) B.四氯化碳(沸点77℃) C.甘油(沸点290℃)
D.苯(沸点80℃)
(3)在操作②中,溶液中生成少量ICl,为消除此杂质,使碘全部游离出来,应加入适量的(填序号) 溶液,反应的离子方程式为 。
A.KIO3 B.KClO C.KI D.Br2
(4)为使从含碘有机溶液中提取碘并回收溶剂顺利进行,采用水浴加热蒸馏(如下图所示)。请指出图中实验装置中错误之处(有几处填几处,下列空白可不填满,也可补充)
① ,② ,③ ,
④ ……

 粤公网安备 44130202000953号
粤公网安备 44130202000953号