2008年全国统一高考化学试卷(江苏卷)
下列溶液中有关物质的量浓度关系正确的是
=2的溶液与=12的溶液任意比混合:() + ()>() + ()
相等的、和三种溶液:()<()<()
物质的量浓度相等和溶液等体积混合:() +()=() + ()
0.1-1的溶液,其=4:()>()>()>()
下列现象或事实可用同一原理解释的是( )
| A. | 浓硫酸和浓盐酸长期暴露在空气中浓度降低 |
| B. | 氯水和活性炭使红墨水褪色 |
| C. | 漂白粉和水玻璃长期暴露会变质 |
| D. | 乙炔和乙烯使溴的四氯化炭溶液褪色 |
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是( )




下列文字表述与反应方程式对应且正确的是( )
| A. | 溴乙烷中滴入 溶液检验其中的溴元素: ↓ |
| B. | 用醋酸除去水垢 ↑ |
| C. | 利用腐蚀法制作印刷线路板: + |
| D. |
实验室用液溴和苯在催化剂作用下制溴苯:
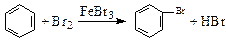
|
在下列溶液中,各组离子一定能够大量共存的是:( )
| A. | 使酚酞试液变红的溶液: 、 、 、 |
| B. | 使紫色石蕊试液变红的溶液: 、 、 、 |
| C. | =10 -12的溶液: 、 、 、 |
| D. | 碳酸氢钠溶液: 、 、 、 |
化学与生活、社会密切相关。下列说法不正确的是( )
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
| B. | 凡含有食品添加剂的食物对人体健康均有害,不可食用 |
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
| D. | 提倡人们购物时不用塑料袋,是为了防止白色污染 |
用表示阿伏加德罗常数的值。下列叙述正确的是( )
| A. | 常温常压下的33.6 氯气与27 铝充分反应,转移电子数为3 |
| B. | 标准状况下,22.4 己烷中共价键数目为19 |
| C. | 由 和 组成的混合物中共有 个分子,其中的氧原子数为2 |
| D. | 1 浓度为1 的 溶液中含有 个 |
以下实验或操作不能达到目的的是
| A. | 用溴水鉴别苯、乙醇、四氯化碳 |
| B. | 准确称取0.4 固体配成1000 浓度为0.01 的溶液 |
| C. | 为除去苯中的少量苯酚,向混合物中加入适量的溴水后过滤 |
| D. | 用激光笔检验淀粉溶液的丁达尔现象 |
将一定量的和含0.7氧气的空气(忽略)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应: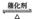 (正反应放热)。反应达到平衡后,将容器中的混合气体通过过量溶液,气体体积减少了21.28;再将剩余气体通过焦性没食子酸的碱性溶液吸收,气体的体积又减少了5.6(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量溶液,气体体积减少了21.28;再将剩余气体通过焦性没食子酸的碱性溶液吸收,气体的体积又减少了5.6(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
 请回答下列问题:
请回答下列问题:



 (1)判断该反应达到平衡状态的标志是。(填字母)
(1)判断该反应达到平衡状态的标志是。(填字母)
 a.和浓度相等 b.百分含量保持不变
a.和浓度相等 b.百分含量保持不变
 c.容器中气体的压强不变 d.的生成速率与的消耗速率相等
c.容器中气体的压强不变 d.的生成速率与的消耗速率相等
 e.容器中混合气体的密度保持不变
e.容器中混合气体的密度保持不变
 (2)欲提高的转化率,下列措施可行的是(填字母)
(2)欲提高的转化率,下列措施可行的是(填字母)
 a.向装置中再充入 b.向装置中再充入
a.向装置中再充入 b.向装置中再充入
c.改变反应的催化剂 d.生高温度
 (3)求该反应达到平衡时的转化率(用百分数表示)。
(3)求该反应达到平衡时的转化率(用百分数表示)。
 (4)若将平衡混合气体的5%通入过量的溶液,生成沉淀多少克?
(4)若将平衡混合气体的5%通入过量的溶液,生成沉淀多少克?
下列离子方程式正确的是()
| A. |
用惰性电极电解饱和氯化钠溶液:

|
| B. |
用银氨溶液检验乙醛中的醛基:

|
| C. |
苯酚钠溶液中通入少量
:

|
| D. | 溶液使酸性 溶液褪色: |
镍镉()可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为溶液,其充、放电按下式进行: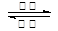 。有关该电池的说法正确的是
。有关该电池的说法正确的是
金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以,和金属离子的配离子的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
①水样预处理:水样中加入磷酸和,在<2的条件下加热蒸馏,蒸出所有的,并用溶液吸收。
②滴定:将吸收液调节至>11,以试银灵作指示剂,用标准溶液滴定
终点时,溶液由黄色变成橙红色。
根据以上知识回答下列问题:
(1)水样预处理的目的是。
(2)水样预处理的装置如右图,细导管插入吸收液中是为了。

(3)蒸馏瓶比吸收液面要高出很多,其目的是。
(4)如果用盐酸代替磷酸进行预处理,实验结果将(填"偏高"、"无影响"或"偏低")。
(5)准确移取某工厂污水100,经处理后用浓度为0.01000的硝酸银标准溶液滴定,终点时消耗了21.00。此水样中含氰化合物的含量为(以计,计算结果保留一位小数)。
根据下列框图回答问题(答题时,方程式中的、用所对应的元素符号表示):

(1)写出溶于稀和混合液的化学方程式:
(2)某同学取的溶液,酸化后加入、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式:、。
(3)写出将氧化为的化学方程式:。
(4)由制备的的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为: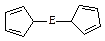 。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有种峰,错误的结构有种峰。
。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有种峰,错误的结构有种峰。
工业上制备的工艺流程图如下:

某研究小组在实验室用重晶石(主要成分)对工业过程进行模拟实验。查表得
①
②
(1)气体用过量溶液吸收,得到硫化钠。水解的离子方程式为。
(2)向溶液中加入和,当两种沉淀共存时,= 。
[=5.4×10-13,=2.0×10-10]
(3)反应的=。
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是。
"温室效应"是全球关注的环境问题之一。是目前大气中含量最高的一种温室气体。因此,控制和治理是解决温室效应的有效途径。
(1)下列措施中,有利于降低大气中浓度的有:。(填字母)
a.减少化石燃料的使用 b.植树造林,增大植被面积
c.采用节能技术 d.利用太阳能、风能
(2)将转化成有机物可有效实现碳循环。转化成有机物的例子很多,如:
a.
b.
c.
d.
以上反应中,最节能的是,原子利用率最高的是。
(3)文献报道某课题组利用催化氢化制甲烷的研究过程如下:

反应结束后,气体中检测到和,滤液中检测到,固体中检测到镍粉和。
、、的产量和镍粉用量的关系如下图所示(仅改变镍粉用量,其他条件不变):
研究人员根据实验结果得出结论:
是转化为的中间体,即:
①写出产生的反应方程式。
②由图可知,镍粉是。(填字母)

a.反应的催化剂
b.反应的催化剂
c.反应的催化剂
d.不是催化剂
③当镍粉用量从1增加到10,反应速率的变化情况是。(填字母)
a.反应Ⅰ的速率增加,反应Ⅱ的速率不变
b.反应Ⅰ的速率不变,反应Ⅱ的速率增加
c.反应ⅠⅡ的速率均不变
d.反应ⅠⅡ的速率均增加,且反应Ⅰ的速率增加得快
e.反应ⅠⅡ的速率均增加,且反应Ⅱ的速率增加得快
f.反应Ⅰ的速率减小,反应Ⅱ的速率增加
布噁布洛芬是一种消炎镇痛的药物。它的工业合成路线如下:
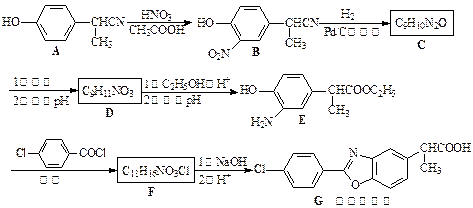
请回答下列问题:
(1)长期暴露在空气中会变质,其原因是。
(2)有到的反应通常在低温时进行。温度升高时,多硝基取代副产物会增多。下列二硝基取代物中,最可能生成的是。(填字母)
a. b.
b. c.
c. d.
d.
(3)在的下列同分异构体中,含有手性碳原子的分子是。(填字母)
a. b.
b.
c. d.
d.
(4)的结构简式。
(5)的同分异构体是一种-氨基酸,可被酸性溶液氧化成对苯二甲酸,则的结构简式是。高聚物由通过肽键连接而成,的结构简式是。
A.已知、、、、都是周期表中前四周期的元素,它们的核电荷数<<<<。其中、、是同一周期的非金属元素。化合物的晶体为离子晶体,的二价阳离子与的阴离子具有相同的电子层结构。为非极性分子。、的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,能与、的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,、、、、用所对应的元素符号表示)
(1)、、的第一电离能由小到大的顺序为
(2)的氢化物的分子空间构型是
(3)写出化合物的电子式
(4)的核外电子排布式是
(5)的最高价氧化物对应的水化物的稀溶液与D的单质反应时,被还原到最低价,该反应的化学方程式是
B.醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
+ +①
+①
+ + ②
+ ②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,-被浓硫酸氧化为等。有关数据列表如下;
| 乙醇 |
溴乙烷 |
正丁醇 |
1-溴丁烷 |
|
| 密度/-3 |
0.7893 |
1.4604 |
0.8098 |
1.2758 |
| 沸点/℃ |
78.5 |
38.4 |
117.2 |
101.6 |
请回答下列问题:
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是
a.圆底烧瓶 b.量筒 c.锥形瓶 d.布氏漏斗
(2)溴代烃的水溶性
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在
(4)制备操作中,加入的浓硫酸必需进行稀释,起目的是
a.减少副产物烯和醚的生成 b.减少的生成
c.减少的挥发 d.水是反应的催化剂
(5)欲除去溴代烷中的少量杂质,下列物质中最适合的是
a.b.c.d.
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于

 粤公网安备 44130202000953号
粤公网安备 44130202000953号