贵州蕴藏丰富的铝、锰、锌、铁、铜等矿产资源。合理开采、充分利用这些矿产资源,可实现“富矿精开”。
Ⅰ.精准识矿
(1)金属的性质与存在形式。
①铝具有很好的抗腐蚀性,因为铝在空气中能与氧气反应形成一层致密的氧化铝薄膜,反应的化学方程式为__________。
②分别在放有锰片、铜片的试管中加入稀硫酸,锰片表面有气泡产生,铜片表面无明显变化。由此可知金属活动性:锰_____(选填“强”或“弱”)于铜。
③在放有锌片的试管中加入硫酸铜溶液,观察到的现象是_____。
多数金属的化学性质比较活泼,它们主要以化合物的形式存在于自然界。如菱锌矿( )、铝土矿( )、菱锰矿( )等。
Ⅱ.精深用矿
(2)工业上用赤铁矿 炼铁, 与 反应的化学方程式为__________。炼铁时,加入菱锰矿可制得冶炼锰钢的材料。锰钢用作高铁的钢轨,利用了锰钢的_____性能。
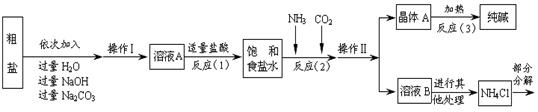
(3)用某菱锰矿为原料制备高附加值新型电池材料 的流程如图1。
已知:菱锰矿中除 外,还有 ; 能与稀硫酸发生复分解反应, 不溶于水也不与稀硫酸反应;氨水呈碱性。

①过滤器中得到的滤渣是_____。
②反应器中, 溶液与 反应可生成锰的氧化物,如 、 、 。发生的反应之一是 , 的化学式是_____。
③ 时,在反应器中保持通入的 和 溶液的质量不变,只改变 溶液的溶质质量分数,测得生成含锰元素的固体中锰元素的质量分数与 溶液的溶质质量分数之间的关系如图2。由图可知,当 溶液的溶质质量分数为 时,可获得高纯度的 ,当 溶液的溶质质量分数为其它数值时, 纯度降低,原因可能是__________。
 8Fe +nCO2+2nH2O,其中n的值为(填数字)。
8Fe +nCO2+2nH2O,其中n的值为(填数字)。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号