硅是信息技术应用的关键材料,徐州已成为单质硅的重要生产基地。工业上常用石英砂(主要成分为 )为原料制得单质硅,主要流程如图所示:
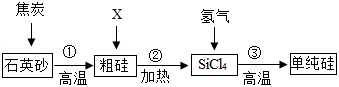
(1)单质硅属于 (填“无机”或“合成”或“复合”)材料。
(2)过程①产生的一种气体,可用作燃料,写出该气体的另一种用途: 。
(3)过程②发生化合反应,参加反应的单质X的化学式为 。
(4)过程③发生置换反应,反应的化学方程式为 。
硅是信息技术应用的关键材料,徐州已成为单质硅的重要生产基地。工业上常用石英砂(主要成分为 )为原料制得单质硅,主要流程如图所示:

(1)单质硅属于 (填“无机”或“合成”或“复合”)材料。
(2)过程①产生的一种气体,可用作燃料,写出该气体的另一种用途: 。
(3)过程②发生化合反应,参加反应的单质X的化学式为 。
(4)过程③发生置换反应,反应的化学方程式为 。