自然界中碳循环如图所示,箭头表示碳的输送途径。
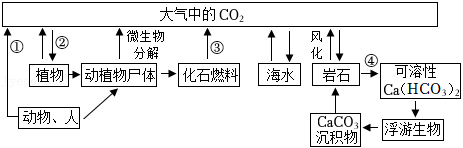
(1)途径①消耗空气中的 。
(2)途径②消耗 的量白天比夜晚 (填“多”或“少”)。
(3)途径③中某气体燃烧的化学方程式为 。
(4)途径④可使空气中 含量 (填“增加”或“减少”)。
(5)“碳中和”指采取各种措施使 排放和消耗基本保持平衡。若要增大途径②碳的消耗量,作为中学生的你能做的是 。
自然界中碳循环如图所示,箭头表示碳的输送途径。

(1)途径①消耗空气中的 。
(2)途径②消耗 的量白天比夜晚 (填“多”或“少”)。
(3)途径③中某气体燃烧的化学方程式为 。
(4)途径④可使空气中 含量 (填“增加”或“减少”)。
(5)“碳中和”指采取各种措施使 排放和消耗基本保持平衡。若要增大途径②碳的消耗量,作为中学生的你能做的是 。