甲、乙、丙三种固体物质的溶解度曲线如图所示。回答下列问题:
(1)在_____ 时,甲、乙的溶解度相等。
(2) 时,将甲溶液的状态由 点变为 点,可采用的方法是_____(回答一种即可)。
(3)将 甲、乙、丙的饱和溶液,分别降温到 ,所得溶液的溶质质量分数最大的是_____。
(4) 时,将等质量的甲、乙、丙的饱和溶液,均恒温蒸发等质量的水,析出溶质质量由多到少的顺序为_____。
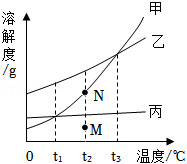
甲、乙、丙三种固体物质的溶解度曲线如图所示。回答下列问题:
(1)在_____ 时,甲、乙的溶解度相等。
(2) 时,将甲溶液的状态由 点变为 点,可采用的方法是_____(回答一种即可)。
(3)将 甲、乙、丙的饱和溶液,分别降温到 ,所得溶液的溶质质量分数最大的是_____。
(4) 时,将等质量的甲、乙、丙的饱和溶液,均恒温蒸发等质量的水,析出溶质质量由多到少的顺序为_____。
