某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法错误的是( )
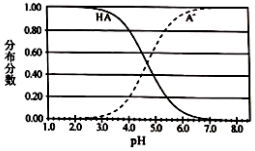
A.该酸﹣lgKa≈4.7
B.NaA的水解平衡常数Kh
C.当该溶液的pH=7.0时,c(HA)<c(A﹣)
D.某c(HA):c(A﹣)=4:1的缓冲溶液,pH≈4
相关知识点
某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法错误的是( )

A.该酸﹣lgKa≈4.7
B.NaA的水解平衡常数Kh
C.当该溶液的pH=7.0时,c(HA)<c(A﹣)
D.某c(HA):c(A﹣)=4:1的缓冲溶液,pH≈4