化学的学科特征是在原子、分子水平上研究物质和创造物质。请从微观的角度回答下列问题。
(1)物质的结构决定性质。
①根据Na、Al原子结构图Na 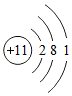 、Al
、Al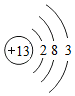 可推知,金属Na、Al的化学性质不同的原因是 。
可推知,金属Na、Al的化学性质不同的原因是 。
②CO和CO2化学性质不同的原因是 。
③稀盐酸和稀硫酸都可使紫色石蕊试剂变红,原因是 。
(2)如图是氢气在氧气中燃烧的微观示意图(图中“o”代表氢原子。“●”代表氧原子)。
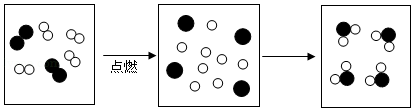
①参加该化学反应的最小粒子是 ( 填微粒符号)。
②写出该反应的化学方程式 。
化学的学科特征是在原子、分子水平上研究物质和创造物质。请从微观的角度回答下列问题。
(1)物质的结构决定性质。
①根据Na、Al原子结构图Na  、Al
、Al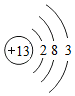 可推知,金属Na、Al的化学性质不同的原因是 。
可推知,金属Na、Al的化学性质不同的原因是 。
②CO和CO2化学性质不同的原因是 。
③稀盐酸和稀硫酸都可使紫色石蕊试剂变红,原因是 。
(2)如图是氢气在氧气中燃烧的微观示意图(图中“o”代表氢原子。“●”代表氧原子)。

①参加该化学反应的最小粒子是 ( 填微粒符号)。
②写出该反应的化学方程式 。