化学在保证人类生存并不断提高生活质量方面起着重要的作用,利用化学综合应用自然资源,以使人类生活得更加美好。目前,人们使用的燃料大多来自化石燃料,如煤、石油、天然气等。煤的综合利用如图所示:
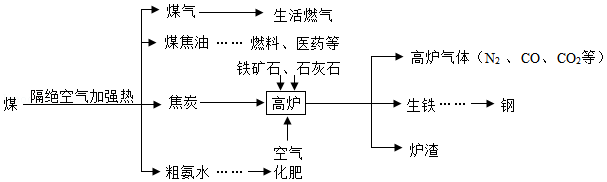
已知高炉内发生的主要化学反应如下:
C+O2 CO2
C+CO2 2CO
3CO+Fe2O3 2Fe+3CO2
(1)将煤隔绝空气加强热的过程是 变化。
(2)粗氨水经提纯后可用作化肥,是因为含有植物所需的 (填元素符号)。
(3)焦炭常作为炼铁工业的原料,请你分析焦炭在炼铁过程中的作用 。
化学在保证人类生存并不断提高生活质量方面起着重要的作用,利用化学综合应用自然资源,以使人类生活得更加美好。目前,人们使用的燃料大多来自化石燃料,如煤、石油、天然气等。煤的综合利用如图所示:

已知高炉内发生的主要化学反应如下:
C+O2 CO2
C+CO2 2CO
3CO+Fe2O3 2Fe+3CO2
(1)将煤隔绝空气加强热的过程是 变化。
(2)粗氨水经提纯后可用作化肥,是因为含有植物所需的 (填元素符号)。
(3)焦炭常作为炼铁工业的原料,请你分析焦炭在炼铁过程中的作用 。