已知A~G均是初中化学常见的物质。A与B的反应在工业上可用于高炉炼铁,B为红棕色固体氧化物,E中含有两种元素,F在农业上可用来改良酸性土壤。它们的相互关系如图所示(“﹣”表示两种物质能发生化学反应,“→”表示一种物质能转化为另一种物质,部分反应物、生成物及反应条件已略去)。请回答:
(1)A﹣B的化学反应方程式为 。
(2)写出D的一种用途: 。
(3)G→A的基本反应类型是 。
(4)C的物质类别是 (填“氧化物”、“酸”、“碱”或“盐”)。
(5)E一F的化学反应方程式为 。
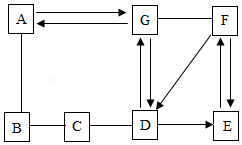
已知A~G均是初中化学常见的物质。A与B的反应在工业上可用于高炉炼铁,B为红棕色固体氧化物,E中含有两种元素,F在农业上可用来改良酸性土壤。它们的相互关系如图所示(“﹣”表示两种物质能发生化学反应,“→”表示一种物质能转化为另一种物质,部分反应物、生成物及反应条件已略去)。请回答:
(1)A﹣B的化学反应方程式为 。
(2)写出D的一种用途: 。
(3)G→A的基本反应类型是 。
(4)C的物质类别是 (填“氧化物”、“酸”、“碱”或“盐”)。
(5)E一F的化学反应方程式为 。
