每年5月31日是“世界禁烟日”。香烟燃烧产生的烟气中含有多种对人体有害的物质,其中的二噁英毒性很强。它是一种无色无味的物质,化学式为C12H4Cl4O2,分子结构如下图所示。通常情况下,它极难溶于水、易溶于脂肪,所以容易在生物体内积累,难以被排出。
回答下列问题:
(1)二噁英属于 (填“无机物”或“有机物”)。
(2)写出二噁英的物理性质: (写出一条即可)。
(3)1个二噁英的分子中含有 个原子,二噁英中碳、氢两种元素的质量比为 。
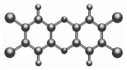
每年5月31日是“世界禁烟日”。香烟燃烧产生的烟气中含有多种对人体有害的物质,其中的二噁英毒性很强。它是一种无色无味的物质,化学式为C12H4Cl4O2,分子结构如下图所示。通常情况下,它极难溶于水、易溶于脂肪,所以容易在生物体内积累,难以被排出。
回答下列问题:
(1)二噁英属于 (填“无机物”或“有机物”)。
(2)写出二噁英的物理性质: (写出一条即可)。
(3)1个二噁英的分子中含有 个原子,二噁英中碳、氢两种元素的质量比为 。
