如图为甲和乙两种固体物质的溶解度曲线.回答下列问题:
(1)t 1℃时,两种物质的饱和溶液中溶质的质量分数较大的是 .
(2)要将t 2℃时甲的饱和溶液变成不饱和溶液,可采取的措施有:增加溶剂、 等.
(3)t 2℃时,在盛有120g蒸馏水的烧杯中,加入80g甲固体,充分溶解后,所得溶液中溶质的质量分数为 .
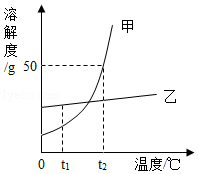
如图为甲和乙两种固体物质的溶解度曲线.回答下列问题:
(1)t 1℃时,两种物质的饱和溶液中溶质的质量分数较大的是 .
(2)要将t 2℃时甲的饱和溶液变成不饱和溶液,可采取的措施有:增加溶剂、 等.
(3)t 2℃时,在盛有120g蒸馏水的烧杯中,加入80g甲固体,充分溶解后,所得溶液中溶质的质量分数为 .
