A、B、C、D、E是初中化学常见的物质,A是大理石的主要成分,E是气体单质,A与B的反应用于实验室制取二氧化碳,它们的相互关系如图所示(图中“﹣”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去)请回答:
(1)E的化学式是 ;
(2)A和B反应的基本反应类型是 反应.
(3)E→C反应的化学方程式为 .
(4)物质D的一种用途是 .
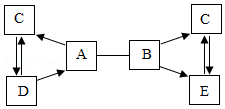
A、B、C、D、E是初中化学常见的物质,A是大理石的主要成分,E是气体单质,A与B的反应用于实验室制取二氧化碳,它们的相互关系如图所示(图中“﹣”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去)请回答:
(1)E的化学式是 ;
(2)A和B反应的基本反应类型是 反应.
(3)E→C反应的化学方程式为 .
(4)物质D的一种用途是 .
