如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
(1)在 ℃时,A和C的饱和溶液中溶质的质量分数相等.
(2)t2℃时,将20gA放入50g水中充分溶解后,所得溶液质量是 g.
(3)若B中含有少量A,可用 的方法提纯B.
(4)将A、B、C的饱和溶液从t3℃降温到t1℃,析出晶体质量最多的是 (填“A”、“B”、“C”或“无法确定”)
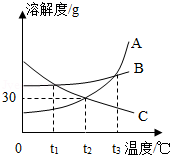
如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
(1)在 ℃时,A和C的饱和溶液中溶质的质量分数相等.
(2)t2℃时,将20gA放入50g水中充分溶解后,所得溶液质量是 g.
(3)若B中含有少量A,可用 的方法提纯B.
(4)将A、B、C的饱和溶液从t3℃降温到t1℃,析出晶体质量最多的是 (填“A”、“B”、“C”或“无法确定”)
