如图是甲、乙、丙三种物质在水中的溶解度曲线,请回答下列问题:
(1)甲、丙两种物质的饱和溶液在 ℃时溶质质量分数相等。
(2)甲中含有少量的乙时,提纯甲的常用方法是 。
(3)t 1℃时各取25g甲、乙、丙三种物质,分别加入到盛有100g水的三只烧杯中,充分溶解后不能形成饱和溶液的是 ,若将温度升至t 3℃时,甲溶液的溶质质量分数将 (填"变大"、"变小"或"不变")。
(4)t 3℃时将等质量的甲、乙、丙三种物质的饱和溶液降温至t 2℃时,所得溶液中溶剂的质量关系是 。
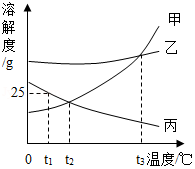
如图是甲、乙、丙三种物质在水中的溶解度曲线,请回答下列问题:
(1)甲、丙两种物质的饱和溶液在 ℃时溶质质量分数相等。
(2)甲中含有少量的乙时,提纯甲的常用方法是 。
(3)t 1℃时各取25g甲、乙、丙三种物质,分别加入到盛有100g水的三只烧杯中,充分溶解后不能形成饱和溶液的是 ,若将温度升至t 3℃时,甲溶液的溶质质量分数将 (填"变大"、"变小"或"不变")。
(4)t 3℃时将等质量的甲、乙、丙三种物质的饱和溶液降温至t 2℃时,所得溶液中溶剂的质量关系是 。
