已知A、B、C、D是初中化学常见的四种物质,在一定条件下它们之间的关系如图(部分物质及反应条件己略去).其中B、C是组成元素相同的气体,D是目前世界年产量最高的金属,A是黑色固体,请回答:
(1)写出下列物质的化学式:A ;B .
(2)C在工业上常用来冶炼D,写出其反应的化学方程式 ,在这个反应中, ___发生了氧化反应.
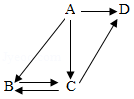
已知A、B、C、D是初中化学常见的四种物质,在一定条件下它们之间的关系如图(部分物质及反应条件己略去).其中B、C是组成元素相同的气体,D是目前世界年产量最高的金属,A是黑色固体,请回答:
(1)写出下列物质的化学式:A ;B .
(2)C在工业上常用来冶炼D,写出其反应的化学方程式 ,在这个反应中, ___发生了氧化反应.
