某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还含有一定量的SiO2)可用于制备FeCO3,其流程如下:
已知:还原时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、II被还原,其中反应Ⅰ为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+。
(1)反应Ⅰ中还原剂是___________________。
(2)滤渣的成分是___________(填名称)。
(3)所得FeCO3需充分洗涤,检验FeCO3是否洗净的方法是__________________。
(4)①配平反应II的离子方程式:_______Fe3++_______FeS2=_______S↓+_______Fe2+。
②还原前后溶液中部分离子的浓度见下表(溶液体积变化忽略不计):
| 离子 |
离子浓度(mol∙L-1) |
|
| 还原前 |
还原后 |
|
| Fe2+ |
0.10 |
2.50 |
| SO42- |
3.50 |
3.70 |
则反应Ⅰ、II中生成Fe2+的物质的量之比为_________。
 CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表:
CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表: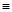 N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________ kJ能量。
N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________ kJ能量。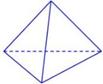

 粤公网安备 44130202000953号
粤公网安备 44130202000953号