处理SO2废气的一种工艺流程如下图所示: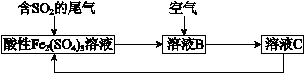
O2是氧化剂;(2)根据(1)的分析,得出:
根据流程,回答下列问题:
(1)溶液B与空气发生反应生成溶液C,其中氧化剂是________。
(2)SO2和酸性Fe2(SO4)3溶液反应的离子方程式是____________________________。
(3)推断Fe3+、O2和SO42−的氧化性由强到弱的顺序是_________________________。
处理SO2废气的一种工艺流程如下图所示:
O2是氧化剂;(2)根据(1)的分析,得出:
根据流程,回答下列问题:
(1)溶液B与空气发生反应生成溶液C,其中氧化剂是________。
(2)SO2和酸性Fe2(SO4)3溶液反应的离子方程式是____________________________。
(3)推断Fe3+、O2和SO42−的氧化性由强到弱的顺序是_________________________。