下表列出了前20号元素中的某些元素性质的有关数据:
元素编号
元素性质
|
①
|
②
|
③
|
④
|
⑤
|
⑥
|
⑦
|
⑧
|
⑨
|
⑩
|
原子半径(10-10m)
|
1.52
|
2.27
|
0.74
|
1.43
|
0.77
|
1.10
|
0.99
|
1.86
|
0.75
|
0.71
|
最高价态
|
+1
|
+1
|
/
|
+3
|
+4
|
+5
|
+7
|
+1
|
+5
|
/
|
最低价态
|
/
|
/
|
-2
|
/
|
-4
|
-3
|
-1
|
/
|
-3
|
-1
|
试回答下列问题:
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是(填写编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式)。某元素R的原子半径为1.02×10-10m,该元素在周期表中位于;若物质Na2R2是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式。
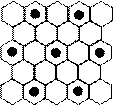
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,该物质的化学式为。