一定条件下,可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压代替平衡浓度计算,分压=总压X物质的量分数。在恒温恒压条件下,总压不变,用平衡分压计算平衡常数更方便。下列说法不正确的是( )
A.对于C2H4 (g) + H2O(g) = C2H5OH(g),在一定条件下达到平衡状态时,体系的总压强为P,其中C2H4(g)、H2O(g)、C2H5OH(g)均为1 mol,则用分压表示的平衡常数Kp = 3/P
B.恒温恒压下,在一容积可变的容器中,反应2A(g)+B(g)=2C(g)达到平衡时,A、B和 C的物质的量分别为4mol、2mol和4mol,若此时A、B和C均增加1mol,平衡正向移动
C.恒温恒压下,在一容积可变的容器中,N2(g)+3H2(g)=2NH3(g)达到平衡状态时,N2、H2、NH3各1mol,若此时再充人3molN2,则平衡正向移动
D.对于一定条件下的某一可逆反应,用平衡浓度表示的平衡常数和用平衡分压表示的平衡常数,其数值不同,但意义相同,都只与温度有关
 时,
时,

 表示,则
表示,则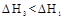
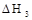 表示,则
表示,则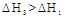
 溶液反应的中和热值为57.3kJ·mol-1
溶液反应的中和热值为57.3kJ·mol-1 ,则反应 HCl(g)=
,则反应 HCl(g)= H2(g) +
H2(g) +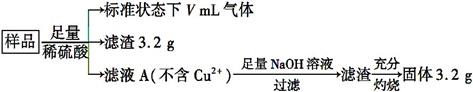
 粤公网安备 44130202000953号
粤公网安备 44130202000953号