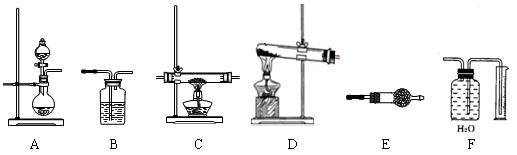
某探究小组用酸性KMnO4溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素。实验条件作如下限定:催化剂的用量可选择0.5g、0g,酸性KMnO4溶液的浓度可选择0.01mol·L﹣1、0.001mol·L﹣1,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4 mL,H2C2O4溶液(0.1mol·L﹣1 )的用量均为2mL。
(1)该反应的离子方程式: 。
(2)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 |
T/K |
催化剂的用量/g |
KMnO4酸性溶液的浓度/mol·L﹣1 |
实验目的 |
| ① |
298 |
0.5 |
0.01 |
(Ⅰ )实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响; (Ⅱ )实验①和③探究温度对该反应速率的影响; (Ⅲ )实验①和 探究催化剂对该反应速率的影响 |
| ② |
|
|
|
|
| ③ |
|
|
|
|
| ④ |
|
|
|
(3)在完成探究催化剂对该反应速率影响的实验时发现,未加催化剂的情况下,刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。针对上述实验现象,同学认为高锰酸钾与草酸溶液的反应放热,导致溶液温度升高,反应速率加快,从影响化学反应速率的因素看,你猜想还可能是 。若用实验证明你的猜想.除酸性高锰酸钾溶液,草酸溶液外,还需要选择的试剂最合理的是 。
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(4)可以利用酸性高锰酸钾测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数,该小组称量2.68 g草酸钠样品溶于稀硫酸中,然后用0.2000 mol·L﹣1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应 )。

①滴定前是否要滴加指示剂? (填“是”或“否” ),当溶液 ,说明滴定达到终点。
②滴定时用 (填a或b )滴定管盛装KMnO4标准溶液。
③达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为 。
 量为17g,则H2R的摩尔质量是,等质量的NH3与H2R的物质的量比为,1.7g氨气与mol H2O含有的电子数相等。
量为17g,则H2R的摩尔质量是,等质量的NH3与H2R的物质的量比为,1.7g氨气与mol H2O含有的电子数相等。

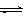 CH3OH(g)+H2O(g) ,△H=-49.0kJ/mol;测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ,△H=-49.0kJ/mol;测得CO2和CH3OH(g)的浓度随时间变化如图所示。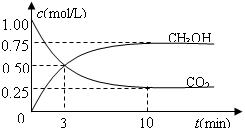
 消除CO的污染。请你判
消除CO的污染。请你判 断是否可行并说出理由: , 。
断是否可行并说出理由: , 。 ;
;
 先通入水中?填“是”或”否”
先通入水中?填“是”或”否” 。
。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号