如图中A到F是化合物,且A、B、E、F均含钠元素,G是单质.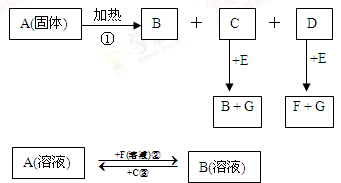
(1)写出A、B、E、F的化学式:A ________,B________,E________,F________.
(2)写出反应①②③的化学方程式:
①______________________________________;
②______________________________________;
③______________________________________。
如图中A到F是化合物,且A、B、E、F均含钠元素,G是单质.
(1)写出A、B、E、F的化学式:A ________,B________,E________,F________.
(2)写出反应①②③的化学方程式:
①______________________________________;
②______________________________________;
③______________________________________。