(1)乙醇的分子结构如右图: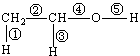 ,其中①②③④⑤表示化学键的代号,用代号回答:
,其中①②③④⑤表示化学键的代号,用代号回答:
i乙醇与钠反应断裂的键是_
ii乙醇与氧气在铜或银作催化剂,加热条件下反应断裂的键是
(2)把一端弯成螺旋状的铜丝放在酒精灯外焰部分加热,看到铜丝表面变成 色。趁热将它反复插入盛乙醇的试管中,铜丝表面又变成 色,并有 气味的物质生成,总反应的化学方程式 。
(1)乙醇的分子结构如右图: ,其中①②③④⑤表示化学键的代号,用代号回答:
,其中①②③④⑤表示化学键的代号,用代号回答:
i乙醇与钠反应断裂的键是_
ii乙醇与氧气在铜或银作催化剂,加热条件下反应断裂的键是
(2)把一端弯成螺旋状的铜丝放在酒精灯外焰部分加热,看到铜丝表面变成 色。趁热将它反复插入盛乙醇的试管中,铜丝表面又变成 色,并有 气味的物质生成,总反应的化学方程式 。