有机物的结构可用“键线式”简化表示.CH3-CH=CH-CH3可简写为 .有机物X的键线式为
.有机物X的键线式为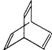
(1)有机物Y是X的同分异构体,且属于芳香烃,请写出Y的结构简式: 。
(2)Y与乙烯在一定条件下发生等物质的量聚合反应,请写出其反应的化学方程式:____________。
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有____种。
有机物的结构可用“键线式”简化表示.CH3-CH=CH-CH3可简写为 .有机物X的键线式为
.有机物X的键线式为
(1)有机物Y是X的同分异构体,且属于芳香烃,请写出Y的结构简式: 。
(2)Y与乙烯在一定条件下发生等物质的量聚合反应,请写出其反应的化学方程式:____________。
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有____种。