用下面的原子或离子结构示意图的编号(A、B、C、D)填空:
A.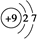 B.
B. C.
C. D.
D.
(1)电子层排布相同的是________________;
(2)属于同种元素的是__________________;
(3)属于金属元素的是____________;其离子的结构示意图___________。
(4)属于稀有气体元素的是________,稀有气体一般不参加化学反应的原因是_____________;
用下面的原子或离子结构示意图的编号(A、B、C、D)填空:
A.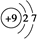 B.
B. C.
C. D.
D.
(1)电子层排布相同的是________________;
(2)属于同种元素的是__________________;
(3)属于金属元素的是____________;其离子的结构示意图___________。
(4)属于稀有气体元素的是________,稀有气体一般不参加化学反应的原因是_____________;