某人设想利用①3FeCl2+4H2O 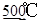 Fe3O4+6HCl+H2
Fe3O4+6HCl+H2
②Fe3O4+3/2Cl2+6HCl 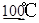 3FeCl3+3H2O +1/2O2
3FeCl3+3H2O +1/2O2
③3FeCl3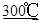 3FeCl2+3/2Cl2
3FeCl2+3/2Cl2
这3个反应的联合与循环,主要用来生产能解决环境和能源问题的某种气体,该气体是
| A.O2 | B.Cl2 | C.H2 | D.HCl |
某人设想利用①3FeCl2+4H2O 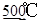 Fe3O4+6HCl+H2
Fe3O4+6HCl+H2
②Fe3O4+3/2Cl2+6HCl 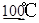 3FeCl3+3H2O +1/2O2
3FeCl3+3H2O +1/2O2
③3FeCl3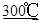 3FeCl2+3/2Cl2
3FeCl2+3/2Cl2
这3个反应的联合与循环,主要用来生产能解决环境和能源问题的某种气体,该气体是
| A.O2 | B.Cl2 | C.H2 | D.HCl |