芳香族化合物A1和A2分别和浓H2SO4在一定温度下共热都只生成烃B,B的蒸气密度是同温同压下H2密度的59倍,B苯环上的一硝基取代物有三种,有关物质之间的转化关系如下:
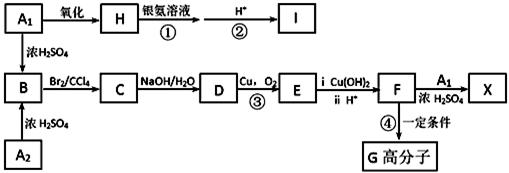
(1)D的分子式为 ,I中官能团名称为 ,
反应③属于__________ 反应(填反应类型)。
(2)写出下列物质的结构简式:A2___________________;X ________________。
(3)写出下列反应的化学方程式:
①________________________________________________________________;
④________________________________________________________________。
(4)化合物J是比化合物E多一个碳原子的E的同系物,化合物J有多种同分异构体,其中同时满足下列条件的同分异构体有 种;
①苯环上有两个取代基;
②能使FeCl3溶液显色;
③与E含有相同官能团
请写出其中核磁共振氢谱图中峰面积比为1:1:2:2:6的结构简式: 。