已知烃A的密度是相同状况下氢气密度的14倍;有机物A-J能发生下图所示一系列变化,其中G、J互为同分异构体。
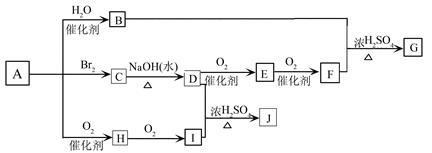
试回答下列问题:
(1)A的化学式: ;G的结构简式:
(2)在A-J的各种物质中,属于醇类是: (填字母,下同);属于醛类的是:
(3)写出下列转化的化学方程式:
C→D:__________
D+I→J:____________
A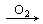 H:__________
H:__________
已知烃A的密度是相同状况下氢气密度的14倍;有机物A-J能发生下图所示一系列变化,其中G、J互为同分异构体。

试回答下列问题:
(1)A的化学式: ;G的结构简式:
(2)在A-J的各种物质中,属于醇类是: (填字母,下同);属于醛类的是:
(3)写出下列转化的化学方程式:
C→D:__________
D+I→J:____________
A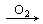 H:__________
H:__________