请认真观察下图,然后回答问题:
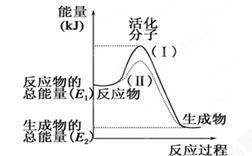
(1)图中所示反应是_______(填“吸热”或“放热”)反应,该反应的ΔH=________(用含E1、E2的代数式表示)。
(2)下列4个反应中,符合示意图描述的反应的是________。
a.盐酸与NaOH反应 b.Na与H2O反应生成H2
c.铝热反应 d.灼热的碳与CO2反应
(3)途径(II)与途径(Ⅰ)相比改变的措施可能是 .
请认真观察下图,然后回答问题:

(1)图中所示反应是_______(填“吸热”或“放热”)反应,该反应的ΔH=________(用含E1、E2的代数式表示)。
(2)下列4个反应中,符合示意图描述的反应的是________。
a.盐酸与NaOH反应 b.Na与H2O反应生成H2
c.铝热反应 d.灼热的碳与CO2反应
(3)途径(II)与途径(Ⅰ)相比改变的措施可能是 .