资料显示:a.Na2S2O3、BaS2O3、BaS均易溶于水。
b.SO2、Na2SO3、Na2CO3反应可生成Na2S2O3。某化学小组据此进行了制备硫代硫酸钠(Na2S2O3)的探究。实验制备装置如图所示(省略夹持装置):
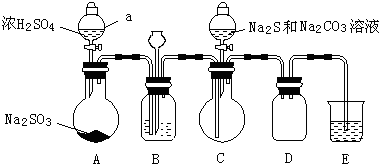
回答问题:
(1)装置A中发生反应的化学方程式是__________________;
(2)装置B的作用之一是观察SO2的生成速率.
①B中最好盛装的液体是____________________;
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
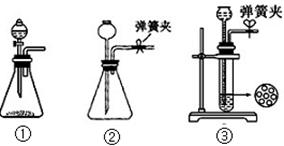
②如使SO2缓慢进入烧瓶C,正确的操作是________________;
(3)在装置C中生成Na2S2O3.
①完成反应方程式:___SO2+_____ Na2S+_____Na2CO3=_____Na2S2O3+ _____
②反应开始先使A中发生反应一会儿,再使C中反应发生,其原因是_______________;
(4)完成对所得产品的检测的实验:
| 推测 |
操作和现象 |
结论 |
| 杂质中的正盐成分可能有:Na2S、Na2CO3、Na2SO4 及___________ |
①取Wg产品配成稀溶液; ②向溶液中滴加过量BaCl2溶液, 有白色沉淀生成,过滤,得沉淀和滤液; ③向沉淀中加入过量盐酸,沉淀完全溶解, 并有刺激性气味的气体产生。 |
产品杂质中: 一定含有________ 可能含有________ 一定不含有_________ |
 CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
 Na2CO3 +CO2↑+H2O
Na2CO3 +CO2↑+H2O



 粤公网安备 44130202000953号
粤公网安备 44130202000953号