I. 对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。下表为几种弱酸在25℃时的电离平衡常数
| 酸 |
电离平衡常数K |
| CH3COOH |
1.76×10-5 |
| H2CO3 |
K1=4.3×10-7 K2=5.61×10-11 |
| H3PO4 |
K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
回答下列问题:
(1)从电离的角度,HCO3-、HPO42-、H2PO4-都可看作是酸,其中酸性最强的是_________,最弱的是________。
(2)等浓度的下列溶液中由水电离出的OH-浓度由大到小的顺序是__(用序号作答)
①CH3COONa ②NaH2PO4 ③NaHPO4 ④NaHCO3 ⑤Na2CO3
(3)电离平衡常数是用实验的方法测定出来的.现已经测得25℃时,c mol/L的 的电离转化率为a,则该温度下醋酸的电离平衡常数KCH3COOH=_____。
的电离转化率为a,则该温度下醋酸的电离平衡常数KCH3COOH=_____。
II.已知t℃时,Kw=1×10 ;在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 a:b=________。
;在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 a:b=________。
III.现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按下图所示步骤进行提纯:

25℃部分阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
| 开始沉淀pH |
2.7 |
7.6 |
4.7 |
| 完成沉淀pH |
3.2 |
9.7 |
6.7 |
请回答下列问题:
(1)流程中加入的试剂a最合适的是_____________(填序号)
A.酸性高锰酸钾溶液 B.NaClO溶液 C.H2O2溶液 D.稀硝酸
加入试剂a的目的是 。
(2)调节pH约4应该加入的物质可以是 。
A.CuO B.CuCl2 C.Cu(OH)2 D.NaOH
利用平衡移动原理简述加入该物质的理由 。
(3)最后能不能直接蒸发结晶得到CuCl2·2H2O?__________(填“能”或“不能”)。如不能,应如何操作?(若能,此空不填) 。

 mol·L-1·min-1
mol·L-1·min-1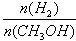 增大
增大 )
) 键和
键和 键数目比为;
键数目比为;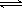 H2(g)+I2(g)已达平衡状态的是
H2(g)+I2(g)已达平衡状态的是
 。该绿色晶体配合物的化学式为
。该绿色晶体配合物的化学式为 粤公网安备 44130202000953号
粤公网安备 44130202000953号