80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4  2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) |
0 |
20 |
40 |
60 |
80 |
110 |
| n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
| n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
①计算20s—40s内用N2O4表示的平均反应速率为 mol/(L.s)
②计算在80℃时该反应的N2O4的转化率= 此温度下
③反应进行至110s后将反应混合物的温度降低,混合气体的颜色 ;如果此时加入NO2,则此时容器内颜色 (填“变浅”、“变深”或“不变”)
④要增大该反应NO2的体积分数,可采取的措施有(填序号)
A.增大N2O4的起始浓度 B.通入N2气体
C.使用高效催化剂 D.升高温度
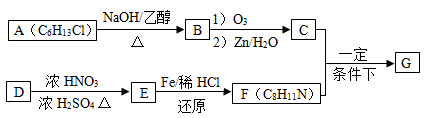




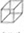 )具有高度的对称性.高致密性.高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点。下面是立方烷衍生物I的一种合成路线:
)具有高度的对称性.高致密性.高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点。下面是立方烷衍生物I的一种合成路线:
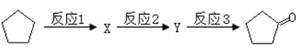
 粤公网安备 44130202000953号
粤公网安备 44130202000953号