利用废铁丝和工业硫酸铜废液(含硫酸亚铁)制备硫酸铜晶体。生产过程如下:
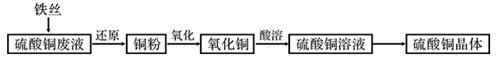
试回答下列问题:
(1)利用硫酸铜的 性质,常在游泳池中加入硫酸铜晶体杀菌消毒。
(2)废铁丝中含有铁锈((Fe2O3・xH2O))在投入硫酸铜废液前需用稀H2SO4进行处理,其主要发生反应的离子方程式_____________________。
(3)铜粉氧化过程中,颜色由粉红变为黑色,再由黑色变绿色。取绿色粉末加入稀硫酸溶液,溶液变蓝,产生无色无味气体,经检验为二氧化碳。推测该绿色粉末为 。(填化学式)
(4)为了使灼烧后的氧化铜混合物充分酸溶,在加入稀H2SO4的同时,还通入O2。通入O2的目的是(用化学反应方程式表示)____________________。
(5)硫酸铜溶液常作电解液,试写出用石墨电极电解硫酸铜溶液阳极反应式: 。
(6)在0.10mol・L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=________________mol・L-1(K sp[Cu(OH)2]=2.2×10-20)。
 2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号