A、B、C、D、E、F六种短周期主族元素,原子序数依次增大,A、B、F三者原子序数之和为25,且知B、F同主族,1.8g E与足量的盐酸反应生成ECl3和2.24L氢气(标准状况下),D+和E的离子具有相同的电子层结构,工业上用电解元素B和E能形成离子化合物的方法冶炼E单质,试判断:
(1)六种元素中非金属性最强的是 (填代号),该元素位于周期表中第 周期第 族;
由A、B、D三种元素形成化合物的电子式
(2)下列能够说明B、F非金属性强弱的方法有
a.最高价氧化物对应水化物酸性
b.气态氢化物的热稳定性
c.气态氢化物的沸点B比F高
d.向F的气态氢化物溶液中通入B单质,有浑浊
(3)写出下列反应的化学方程式
①E与足量的盐酸反应的化学方程式
②写出足量D的最高价氧化物对应水化物与ECl3相互反应的离子方程式
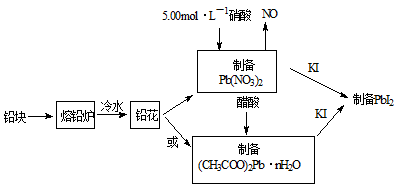
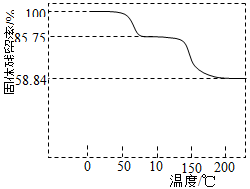
 )随温度的变化如下图所示(已知:样品在75℃时已完全失去结晶水)。
)随温度的变化如下图所示(已知:样品在75℃时已完全失去结晶水)。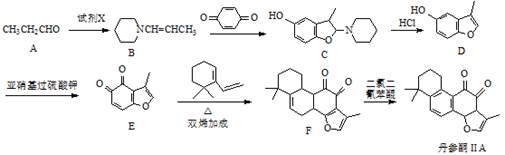
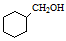 的合成路线流程图(无机试剂可任选)。合成路线流程图示例如下:
的合成路线流程图(无机试剂可任选)。合成路线流程图示例如下: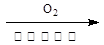 CH3COOH
CH3COOH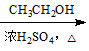 CH3COOCH2CH3
CH3COOCH2CH3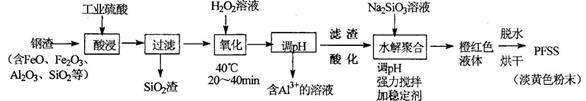
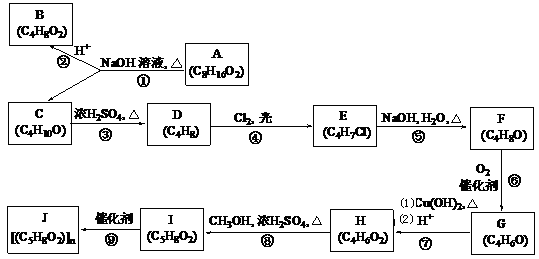
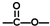 ”结构的链状化合物共有________种;写出(i)能发生水解反应
”结构的链状化合物共有________种;写出(i)能发生水解反应 粤公网安备 44130202000953号
粤公网安备 44130202000953号