美国化学家设计出以甲烷等碳氢化合物为燃料的新型电池,其成本大大低于以氢为燃料的传统电池。燃料电池使用气体燃料和氧气直接反应产生电能,其效率高、污染低,是一种很有前途的能源利用方式。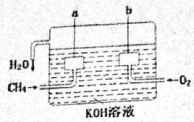
(1)用KOH溶液做电解质,甲烷燃料电池的总反应方程式为______________;
(2)a是电池的____极,电极反应式为____________;
(3)标准状况时,通入甲烷1.12L,理论上通过导线的电子的数目为_______。
美国化学家设计出以甲烷等碳氢化合物为燃料的新型电池,其成本大大低于以氢为燃料的传统电池。燃料电池使用气体燃料和氧气直接反应产生电能,其效率高、污染低,是一种很有前途的能源利用方式。
(1)用KOH溶液做电解质,甲烷燃料电池的总反应方程式为______________;
(2)a是电池的____极,电极反应式为____________;
(3)标准状况时,通入甲烷1.12L,理论上通过导线的电子的数目为_______。