乙炔是一种重要的有机化工原料,以乙炔为原料在不同的条件下可以转化成以下化合物。完成下列各题:
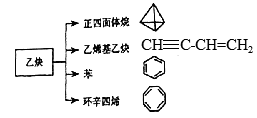
(1)正四面体烷的分子式为________。
(2)关于乙烯基乙炔分子的说法错误的是_____:
a.能使酸性KMnO4溶液褪色
b.1 mol乙烯基乙炔能与3molBr2发生加成反应
c.生成乙烯基乙炔分子的反应属于取代反应
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:__________。
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的条件下可以转化成以下化合物。完成下列各题:
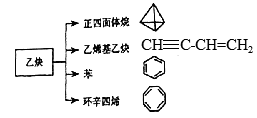
(1)正四面体烷的分子式为________。
(2)关于乙烯基乙炔分子的说法错误的是_____:
a.能使酸性KMnO4溶液褪色
b.1 mol乙烯基乙炔能与3molBr2发生加成反应
c.生成乙烯基乙炔分子的反应属于取代反应
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:__________。