一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g) 2C(g)△H<0,反应过程中B、C的物质的量随时间变化关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图下列有关说法不正确的
2C(g)△H<0,反应过程中B、C的物质的量随时间变化关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图下列有关说法不正确的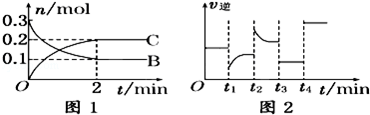
A.反应开始2分钟内,v(B)=0.05mol/(L•min)
B.t1时改变的条件可能是减小了反应物的浓度
C.t2时可能升高了温度,t3时改变的条件可能是降压,此时c(B)减小
D.T4时可能使用了催化剂
一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g) 2C(g)△H<0,反应过程中B、C的物质的量随时间变化关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图下列有关说法不正确的
2C(g)△H<0,反应过程中B、C的物质的量随时间变化关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图下列有关说法不正确的
A.反应开始2分钟内,v(B)=0.05mol/(L•min)
B.t1时改变的条件可能是减小了反应物的浓度
C.t2时可能升高了温度,t3时改变的条件可能是降压,此时c(B)减小
D.T4时可能使用了催化剂