白云石的主要成份是CaCO3·MgCO3,在我国有大量的分布。以白云石为原料生产的钙镁系列产品有广泛的用途。白云石经煅烧、熔化后得到钙镁的氢氧化物,再经过碳化实现Ca2+、Mg2+的分离。
已知:碳化反应是放热反应,化学方程式Ca(OH)2+Mg(OH)2+3CO2 CaCO3+Mg(HCO3)2+H2O。完成下列填空:
CaCO3+Mg(HCO3)2+H2O。完成下列填空:
(1)Ca(OH)2的碱性比Mg(OH)2的碱性 (填“强”或“弱”)
Ca(OH)2的溶解度比Mg(OH)2的溶解度 (填“大”或“小”)。
(2)碳化温度保持在50~60℃。温度偏高不利于碳化反应,原因是 、 (至少写2点)。温度偏低也不利于碳化反应,原因是 。

(3)已知某次碳化时溶液中钙离子浓度随时间的变化如图所示,在10min到13min之内钙离子的反应速率为 。用化学方程式表示15min之后钙离子浓度增大的原因 。
 C(g)+D(g)ΔH<0。请回答下列问题:
C(g)+D(g)ΔH<0。请回答下列问题: CH3OH(g)。请根据图示回答下列问题:
CH3OH(g)。请根据图示回答下列问题: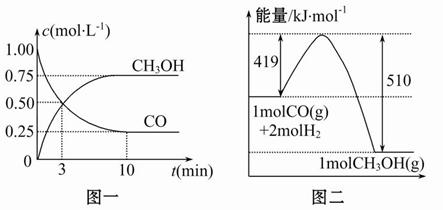
 Fe(s)+CO2(g)ΔH>0,已知1 373 K时K=0.263。
Fe(s)+CO2(g)ΔH>0,已知1 373 K时K=0.263。 2NO2(g)在前110 s内的反应进行情况,请根据图像回答下列问题。
2NO2(g)在前110 s内的反应进行情况,请根据图像回答下列问题。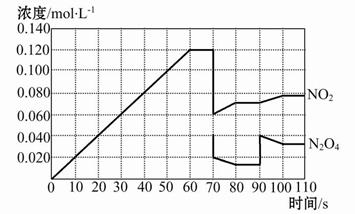
 粤公网安备 44130202000953号
粤公网安备 44130202000953号