(1)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出热量649.5 中kJ,其热化学方程为 。
又已知:H2O(l)=H2O(g);ΔH=+44.0kJ/mol。则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量为 。
恒温、恒压(1.01×105Pa)下,将2.0molSO2与amolO2的混合气体通入一个容积可变的密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g);ΔH<0
2SO3(g);ΔH<0
(2)T1℃下反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol,则a=__________;平衡时SO2的转化率为_________。T2℃下反应达平衡时,混合气体的物质的量共为4.8mol.T1与T2的关系是________(选填序号)。
①T1>T2 ②T1<T2 ③T1=T2

 CH3OH(g)ΔH
CH3OH(g)ΔH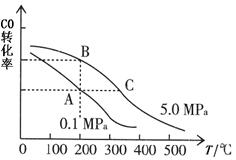
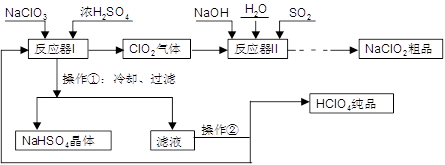
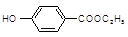 ,生产过程如下图:
,生产过程如下图: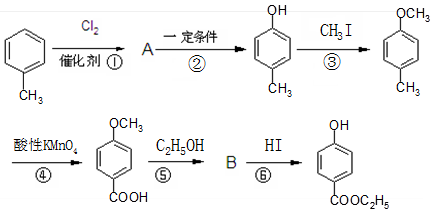
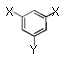 ,-X、-Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,则-X的结构简式可能是、。
,-X、-Y为取代基)是对羟基苯甲酸乙酯的同分异构体且能发生银镜反应,则-X的结构简式可能是、。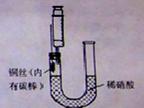
 N2O4(g) △H <0;N2O4为无色气体。
N2O4(g) △H <0;N2O4为无色气体。 粤公网安备 44130202000953号
粤公网安备 44130202000953号