已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是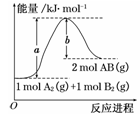
| A.每生成2分子AB吸收b kJ热量 |
| B.该反应热ΔH=+(a-b) kJ·mol-1 |
| C.该反应中反应物的总能量高于生成物的总能量 |
| D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量 |
已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是
| A.每生成2分子AB吸收b kJ热量 |
| B.该反应热ΔH=+(a-b) kJ·mol-1 |
| C.该反应中反应物的总能量高于生成物的总能量 |
| D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量 |